
| A. | Br2>Fe2+>I2 | B. | Br2>Fe3+>I2 | C. | I2>Br2>Fe3+ | D. | Fe3+>Br2>I2 |
分析 根据元素的化合价升高来判断还原剂,利用氧化还原反应中还原剂的还原性大于还原产物的还原性来解答.
解答 解:2Fe3++2I-=2Fe2++I2中,I元素的化合价升高,由还原剂的还原性大于还原产物的还原性,则还原性I->Fe2+,所以氧化性Fe3+>I2;
Br2+2Fe2+=2Fe3++2Br-中,Fe元素的化合价升高,由还原剂的还原性大于还原产物的还原性,则还原性Fe2+>Br-,所以氧化性Br2>Fe3+;
所以离子的还原性由强到弱的顺序为I->Fe2+>Br-,氧化性强弱为:Br2>Fe3+>I2,
故选B.
点评 本题考查离子还原性的比较,明确氧化还原反应中还原剂中元素的化合价升高、还原剂的还原性大于还原产物的还原性,氧化剂的氧化性强于氧化产物的氧化性即可解答.


科目:高中化学 来源: 题型:选择题
| A. | 天然蛋白质的水解产物是多种a-氨基酸 | |
| B. | 蛋白质溶液里加入饱和硫酸铵溶液,蛋白质会析出,且加水也不溶解 | |
| C. | 重金属盐能使蛋白质凝结,所以误食重金属盐会中毒 | |
| D. | 浓硝酸沾到皮肤上能使浓硝酸和蛋白质发生颜色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 25.02 |
| 2 | 20.00 | 0.20 | 28.80 |
| 3 | 20.00 | 1.30 | 26.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下所有的金属都是固态 | |
| B. | 金属具有导电、导热和延展性 | |
| C. | 金属元素的原子只有还原性,离子只有氧化性 | |
| D. | 所有金属元素都以化合态存在于自然界 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时可用水扑灭 | |
| B. | 酒精灯着火时用湿抹布扑盖 | |
| C. | 蒸发结晶时,为得到更多晶体直接将溶液蒸干 | |
| D. | 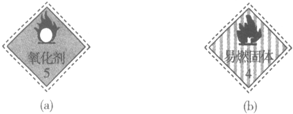 实验室可分别将贴有标志(a)和标志(b)的药品放在同一橱柜中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢气体不能导电,所以氯化氢不是电解质 | |
| B. | SO2溶于水形成的溶液能导电,所以SO2是电解质 | |
| C. | 碳棒能导电但属于非电解质 | |
| D. | 电解质不一定能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T1℃时,在1L密闭容器中充入0.6molSO3,如图表示SO3物质的量随时间的变化曲线.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T1℃时,在1L密闭容器中充入0.6molSO3,如图表示SO3物质的量随时间的变化曲线.| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com