
【题目】浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
A | B | C | D | |
溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |

A.AB.BC.CD.D
【答案】BD
【解析】
A.浓度为0.1mol/L的盐酸,滴加同浓度的氢氧化钠溶液,生成氯化钠,溶液的体积变大,导致离子浓度减小,导电能力减弱,故A错误;
B.醋酸是弱电解质部分电离,向其中滴入氢氧化钠,生成的醋酸钠为强电解质,自由移动离子浓度增大,导电能力增强,故B正确;
C.氢氧化钠和氨水不反应,氨水是弱电解质,向氢氧化钠溶液中滴入氨水,相当于对氢氧化钠稀释,离子浓度减小,导电能力减弱,故C错误;
D.向氨水中滴入硝酸银,形成银铵络离子,先产生白色沉淀AgNO3+NH3H2O=AgOH+NH4NO3,继续滴加氨水,沉淀消失,发生AgOH+2NH3H2O=[Ag(NH3)2]OH +2H2O,而[Ag(NH3)2]OH是一元强碱,导致离子浓度增大,导电能力增强,故D正确;
选BD。


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
【题目】今有甲、乙、丙三瓶等体积的新制的氯水,浓度均为0.1molL-1。如果在甲瓶中加入少量的NaHCO3晶体(mmol),在乙瓶中加入少量NaHSO3(mmol),丙瓶不变,片刻后甲、乙、丙三瓶溶液中HClO的物质的量的浓度大小关系是(溶液体积变化忽略不计)( )
A.甲=乙>丙B.甲>乙>丙C.丙>甲=乙D.甲>丙>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00 L的密闭容器中,充入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随着温度升高,混合气体的颜色变深。体系中各物质的浓度变化与时间关系如图所示。下列说法正确的是
2NO2(g),随着温度升高,混合气体的颜色变深。体系中各物质的浓度变化与时间关系如图所示。下列说法正确的是
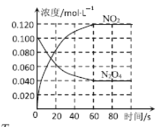
A.反应的△H <0
B.在 060s 时段,反应速率v(N2O4)=0.001mol·L-1·s-1
C.平衡时,反应的平衡常数K=0.240
D.T1℃时平衡后将温度变为T2℃,测得c(N2O4)降低,则T1>T2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2HI(g)![]() H2(g)+I2(g) △H=Q,在4种不同条件下进行,已知起始时I2与H2的物质的量为0,反应物HI的浓度(mol/L)随反应时间(min)的变化情况如下表所示:
H2(g)+I2(g) △H=Q,在4种不同条件下进行,已知起始时I2与H2的物质的量为0,反应物HI的浓度(mol/L)随反应时间(min)的变化情况如下表所示:
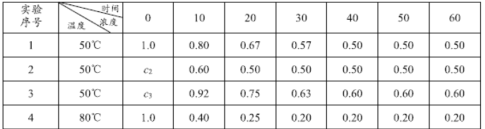
(1)实验1中,反应在010 min内平均速率v(HI)为_______mol·L-1·min-1。仔细分析上表数据可推知Q ______0 (填“>”“<”或“=”)。
(2)实验2中,HI的初始浓度c2 为_____mol·L-1.设平衡前实验1的平均反应速率为v1,平衡前实验3的平均反应速率为v3,则v1 ____v3 (填“>”“<”或“=”),且 c3为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知蓄电池在充电时作电解池,放电时作原电池.如图是铅蓄电池的工作示意图,其反应原理为:PbO2+Pb+2H2SO4![]() 2PbSO4+2H2O下列说法中错误的是( )
2PbSO4+2H2O下列说法中错误的是( )

A.b电极放电后转化为c电极
B.电极a和d都发生还原反应
C.b的电极反应式:Pb+SO42﹣﹣2e-→PbSO4
D.放电后硫酸溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“苏丹红一号”(结构如下图所示)是一种合成染料,科学家通过经毒理学研究,发现长期食用含有苏丹红的食品对人体可能有致癌因素。下列关于“苏丹红一号”的说法中不正确的是

A. 属于芳香族化合物,分子式为C16H12N2O
B. 分子中的所有原子可能位于同一平面上
C. 分子中苯环上的一取代物共有11种
D. 能与NaOH溶液、FeCl3溶液、溴水等物质反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种有机物:①乙烯 ②2-丙醇 ③ 甲苯 ④ 乙炔,其中:
(1)能发生消去反应的是_________(填序号,下同),其化学方程式是________。
(2)能衡量一个国家的石油化工生产水平的是__________,该物质可用于一种常用塑料,其反应的化学方程式是__________。
(3)能用来制取梯恩梯(TNT)的是________,其发生反应的化学方程式是________。
(4)碳元素的质量百分含量最高的是________,实验室制取该物质的反应装置如下:
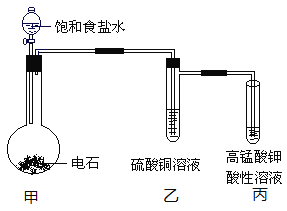
甲中反应的化学方程式是________,滴加饱和食盐水而不直接滴加水的原因是________,乙中硫酸铜溶液的作用是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com