
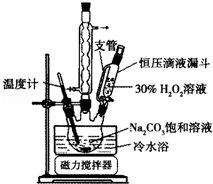
 2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.
2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.分析 Ⅰ.(1)球形冷凝管可使液体冷凝回流;冷水浴降低温度,防止物质分解;
(2)加入适量NaCl固体,发生盐析;
(3)2Na2CO3•3H2O2极易分解,生成碳酸钠、氧气、水;
Ⅱ.(4)高锰酸钾标准溶液为紫色,与过氧化氢发生氧化还原反应;活性氧含量计算公式:Q%=$\frac{40cV}{m}$×100%,以此计算;
Ⅲ.(5)方案中可测定过氧化氢分解生成的氧气,或测定碳酸根离子转化生成的沉淀或气体来测定产品中2Na2CO3•3H2O2的质量分数.
解答 解:Ⅰ.(1)装置中球形冷凝管的作用是起冷凝回流的作用,过氧化氢不稳定,则使用冷水浴的作用是防止温度过高,H2O2分解,
故答案为:起冷凝回流的作用,防止温度过高,H2O2分解;
(2)加入适量NaCl固体,降低产品的溶解度(盐析作用)或便于析出晶体,故答案为:降低产品的溶解度(盐析作用)或便于析出晶体;
(3)2Na2CO3•3H2O2极易分解,生成碳酸钠、氧气、水,反应方程式为2(2Na2CO3•3H2O2)═4Na2CO3+6H2O+3O2↑,
故答案为:2(2Na2CO3•3H2O2)═4Na2CO3+6H2O+3O2↑;
Ⅱ.(4)高锰酸钾标准溶液为紫色,能与过氧化氢发生氧化还原反应,高锰酸钾标准溶液滴定2Na2CO3•3H2O2,则滴定终点的判断依据为溶液由无色呈紫色且30s内不褪色,0.0200mol/L高锰酸钾标准溶液消耗的体积为32.70mL,试样0.2000g,活性氧含量为Q%=$\frac{40cV}{m}$×100%=$\frac{40×0.020mol/L×0.03270L}{0.200g}$×100%=13.08%,
故答案为:溶液由无色呈紫色且30s内不褪色,13.08%;
Ⅲ.(5)方案中可测定过氧化氢分解生成的氧气,或测定碳酸根离子转化生成的沉淀(或气体体积)质量测定产品中2Na2CO3•3H2O2的质量分数,则方案二为将试样与足量的氯化钡(或氯化钙等)溶液反应后,过滤,干燥所得沉淀,称量沉淀的质量(或试样与足量稀硫酸反应后,经除杂干燥后,测二氧化碳的体积,进行计算),
故答案为:将试样与足量的氯化钡(或氯化钙等)溶液反应后,过滤,干燥所得沉淀,称量沉淀的质量(或试样与足量稀硫酸反应后,经除杂干燥后,测二氧化碳的体积,进行计算).
点评 本题考查制备实验方案的设计,为高频考点,把握实验基本操作、实验技能及测定原理、发生的反应等为解答的关键,侧重分析与实验能力的考查,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、OH-、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H=-akJ•mol-1,则中和热为a/2kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l);△H1=-akJ•mol-1,则氢气燃烧热为akJ•mol-1 | |
| C. | 反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 | |
| D. | N2(g)+3H2(g)?2NH3(g);△H=-akJ•mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 石英可用于制作光导纤维,光导纤维遇强碱会“断路” | |
| C. | 清晨阳光穿过林木枝叶铺洒地面属于丁达尔现象 | |
| D. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某H2S04溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×l0-8,由水电离出的c(H+)=1×10-11 mol•L-1 | |
| B. | 将0.02 mol.L-1 HCI溶液与0.02 mol•L-l Ba( OH)2溶液等体积混合后,溶液pH约为12 | |
| C. | 将一定体积稀盐酸与稀氨水混合,当溶质为NH3•H20和NH4Cl时,溶液的pH≥7 | |
| D. | 向0.1 mol•L-1 Na2C03溶液中逐滴滴加0.1 mol•L-1稀盐酸,溶液中c(HCO3-)先增大后减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、SO42-、CO32-、K+ | B. | Na+、Ba2+、Ca2+、HCO3- | ||
| C. | Mg2+、Ag+、K+、Cl- | D. | K+、Cl-、Na+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 图是2008年北京奥运会的“祥云”火炬,与悉尼奥运火炬所用主要燃料(丁烷)不同,“祥云”火炬所用燃料为丙烷.丙烷和丁烷的沸点如下表:
图是2008年北京奥运会的“祥云”火炬,与悉尼奥运火炬所用主要燃料(丁烷)不同,“祥云”火炬所用燃料为丙烷.丙烷和丁烷的沸点如下表:| 丙烷 | 丁烷 | |
| 沸点/℃ | -42.6 | -0.5 |
| A. | 丙烷燃烧生成的产物无害,是环保型燃料 | |
| B. | 丙烷的沸点比丁烷低,是因为分子间作用力比丁烷弱 | |
| C. | 丙烷在低温时保持的压力比丁烷大 | |
| D. | 丙烷和丁烷都不存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
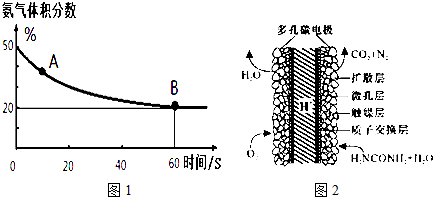
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com