
| A、①④ | B、②④ | C、①③ | D、②⑤ |
| c(Na+) |
| c(HCO3-) |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、M两种元素只能形成X2M型化合物 |
| B、由于W、Z、M元素的氢化物的相对分子质量依次减小,所以其沸点依次降低 |
| C、元素X、Z、W的单质晶体中含相同类型的化学键 |
| D、元素W和M的某些单质可作为水处理中的消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
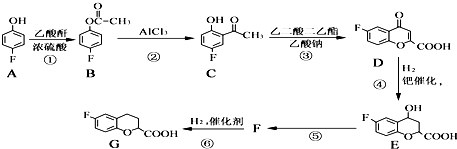
 请回答下列问题:
请回答下列问题: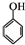 和乙酸酐为原料制备
和乙酸酐为原料制备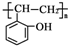 的合成路
的合成路查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2+HNO3+H2O |
| B、N2+NH3+H2O |
| C、NH3+HNO3 |
| D、NH3+NO+H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com