
某化学兴趣小组利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气发生反应的装置.
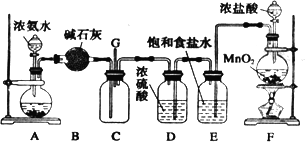
请回答下列问题:
(1)装置A中的固体物质不宜选用________(填字母编号).
a.无水氯化钙
b.氢氧化钠
c.氧化钙
d.碱石灰
e.无水硫酸铜
(2)写出装置F中发生反应的离子方程式:________;
E装置的作用为________.
(3)通入C装置的两根导管左边较长、右边较短,原因是________.
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.当有0.15 mol Cl2参与反应时,则生成的气体在标准状况下的体积为________.
(5)上述装置还存在一处明显的缺陷,你认为改进的措施是________.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用热的纯碱溶液洗涤餐具上的油污 | B、用食醋除去暖水瓶内的薄层水垢 | C、用米汤检验食盐中是否含有碘酸钾 | D、用灼烧并闻气味的方法鉴别纯棉织物和纯羊毛织物 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省稳派名校学术联盟高三12月调研考试理综化学试卷(解析版) 题型:填空题
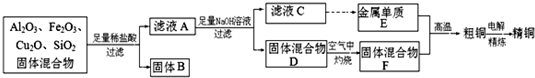
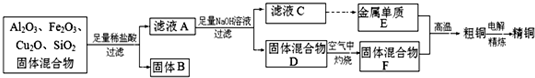
某化学兴趣小组利用废弃铝矿(含CuO、Al2O3及SiO2),模拟工业上提取铝的工艺,设计如下图所示的简单操作流程:
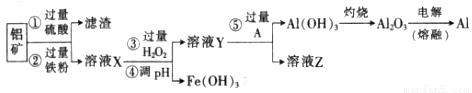
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
|
沉淀物 |
|
|
|
|
开始沉淀 |
2.3 |
7.5 |
3.4 |
|
完全沉淀 |
3.2 |
9.7 |
4.4 |
回答下列问题:
(1)滤渣主要成分的化学式为______________________。
(2)灼烧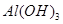 时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有___________(填仪器名称)。
时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有___________(填仪器名称)。
(3)溶液Y中要加入稍过量原料A,原料A的化学式是_________,步骤⑤反应的离子方程式是_______________________。
(4)操作流程中③的离子方程式为_______________________。
(5)铝电池性能优越,Al—Ag2O电池可用作水下动力电源,其原理如图所示:
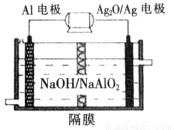
请写出该电池正极反应式_________________;常温下,用该化学电源和惰性电极电解300mL氯化钠溶液(过量),消耗27mg Al,则电解后溶液的pH=_________(不考虑溶液体积的变化)。
(6)以熔融盐为电镀液可以在钢材表面镀铝,镀铝电解池中,钢材为________极;镀铝后能防止钢材腐蚀,其原因是____________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年安徽省“江南十校”高三第一次模拟考试化学试卷(解析版) 题型:实验题
氧化铜是一种黑色粉末,其制品除在烟花中使用外还可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂。为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源回收再利用,减少污染。
(1)获得硫酸铜
该小组同学利用H2O2和H2SO4混合溶液可溶出印刷电路板金属粉末中的铜,从而获得硫酸铜。
写出该反应的化学方程式 。
(2)制备氧化铜

①步骤I的目的是除去可溶性杂质;
②步骤II的目的是得到CuSO4·5H2O固体。该步骤操作是 、 、过滤、水浴加热烘干。水浴加热的特点是 。
(3)探究氧化铜是否能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。用如图装置进行实验,实验时均以收集25mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
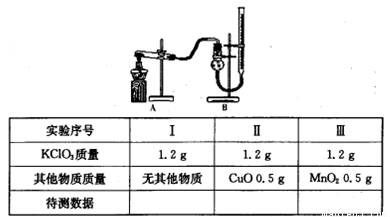
回答下列问题:
①上述实验中的“待测数据”指 。
②若要证明实验II中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞, 。
③为探究CuO在实验III中是否起催化作用,需补做如下实验(无需写出具体操作):
a.CuO的化学性质有没有改变;b 。.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com