
现有等物质的量的铜和银的混合物17.2克,与50.0mL的浓硝酸恰好完全反应,产生气体4.48L(标准状况),则下列说法正确的是
| A.产生的气体是0.2molNO2 |
| B.硝酸的物质的量浓度为12mol/L |
| C.反应中被还原和未被还原的硝酸物质的量之比为3:2 |
| D.要使产生的气体恰好完全被水吸收需要通入氧气0.075mol |
科目:高中化学 来源: 题型:单选题
根据表中信息判断,下列选项正确的是( )
| A.第①组反应的其余产物为H2O |
| B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1:2 |
| C.第③组反应中生成1mol Cl2,转移电子5mol |
| D.氧化性由强到弱顺序为MnO4 >Cl2> Fe3+> Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实不能说明元素的金属性或非金属性相对强弱的是
| 序号 | 事实 | 推论 |
| A | 与冷水反应,Na比Mg剧烈 | 金属性:Na > Mg |
| B | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca > Mg |
| C | SO2与NaHCO3溶液反应生成CO2 | 非金属性:S > C |
| D | t℃时,Br2 + H2 2HBr K = 5.6×107 2HBr K = 5.6×107I2 + H2  2HCl K = 43 2HCl K = 43 | 非金属性:Br > I |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | | FeBr2 | / | | Cl- |
| ② | MnO2 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
KClO3与浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,有关该反应,说法不正确的是:( )
| A.被氧化的元素和被还原的元素的质量之比5:1 |
| B.Cl2既是氧化产物,又是还原产物 |
| C.盐酸既体现酸性,又体现酸性还原性 |
| D.转移5mol电子时,产生67.2L的Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
| A.a原子的最外层电子数比b原子的最外层电子数少 |
| B.把a、b两块金属片浸入稀硫酸中,用导线相连组成原电池时,电流由 a到b |
| C.1mol a 从酸中置换H+生成的H2比1 mol b从酸中置换H+生成的H2多 |
| D.常温时,a能从水中置换出氢,而b不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某反应的反应物与生成物有:K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知反应过程中发生如下变化:K2Cr2O7→CrCl3,则下列说法不正确的是
| A.由此反应可知氧化性K2Cr2O7>Cl2 |
| B.氧化剂和还原剂的物质的量之比为1:6 |
| C.当转移0.2mol电子时,生成的还原产物的物质的量为0.1mol |
| D.发生氧化还原反应的氯元素与参加反应的氯元素的比为3:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知常温下在溶液中可发生如下两个离子反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是
| A.Sn2+、Fe2+、Ce3+ | B.Sn2+、Ce3+、Fe2+ |
| C.Ce3+、Fe2+、Sn2+ | D.Fe2+、Sn2+、Ce3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示。下列说法中不正确的是( )。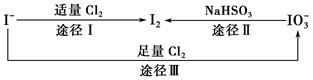
| A.用淀粉—KI试纸和食醋检验加碘盐时淀粉—KI试纸会变蓝 |
| B.足量Cl2能使湿润的、已变蓝的淀粉—KI试纸退色的原因可能是5Cl2+I2+6H2O=2HIO3+10HCl |
| C.由图可知氧化性的强弱顺序为Cl2>I2>IO3- |
| D.途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com