
| A、红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| B、钠在氯气中燃烧,生成白色的烟 |
| C、纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色的烟 |
| D、氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |


科目:高中化学 来源: 题型:


| 充电 |
| 放电 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH<7的溶液中:SO32-、Cu2+、HClO、K+ |
| B、加入铝粉后产生大量氢气的溶液中:Fe3+、Na+、NO3-、SO42- |
| C、无色透明溶液中:[Ag(NH3)2]+、NH3?H2O、OH-、NO3- |
| D、常温下,水电离出的c(H+)=10-14 mol?L-1的溶液中:Na+、Ca2+、Br-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若a=b,则混合后溶液的pH<7 |
| B、若混合后溶液pH=7,则c(M+)>c(Cl-) |
| C、若a=2b,则c(M+)>c(Cl-)>c(MOH)>c(OH-)>c(H+) |
| D、若混合后溶液满足c(H+)=c(OH-)+c(MOH),则可推出a=b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2种 | B、5种 | C、4种 | D、6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.4×10-7mol?L-1 |
| B、0.1×10-7mol?L-1 |
| C、4.2×10-8mol?L-1 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、Na+、SO42-、OH- |
| B、Ag+、NH3?H2O、NO3- |
| C、Ba2+、H+、NO3-、PO43- |
| D、Na+、Al3+、Cl-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
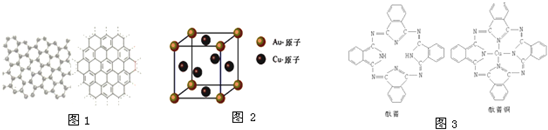
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com