
����Ŀ���й���ѧԺ��ѧ���Ŷ�ͨ��þ�Ȼ�ԭ������Ȼ�Ĺ�����ת��Ϊ���ж༶���ṹ�Ĺ��ܣ������ù���������̬��﮽�������Ƴɾ��ж�ṹ�ĸ���﮽�����һ��ȫ��̬﮽���������Ը���﮽���Ϊa�����������Ϊb�����ۻ���������ۺ���(PEO-SPE)Ϊ��̬�����(��ͼ��ʾ)���õ�ص��ܷ�ӦΪ��LiFePO4![]() xLi+Li1-xFePO4������˵������ȷ
xLi+Li1-xFePO4������˵������ȷ
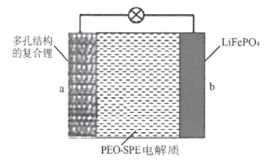
A.�ŵ�ʱLi+ͨ����̬�������b���ƶ�
B.��ṹ�ĸ���﮽���������﮽����ľ��ȳ������ѳ�
C.���ʱ��b����ӦΪ��Li1-xFePO4+xe-+xLi+=LiFePO4
D.���ʱ����a����������mgʱ��������b����������mg
���𰸡�C
��������
�ŵ�ʱ����װ��Ϊԭ���װ�ã�����﮽���(a)Ϊ������������ӦΪ��xLi-xe-=xLi+���������Ϊ(b)������������ӦΪ��Li1-xFePO4+xLi++xe-= LiFePO4��
���ʱ����װ��Ϊ����װ�ã�����﮽���(a)Ϊ������������ӦΪ��xLi++xe-=xLi���������(b)Ϊ������������ӦΪ��LiFePO4-xe-= Li1-xFePO4+xLi+���ݴ˽��
A���ŵ�ʱ����װ��Ϊԭ���װ�ã��������������ƶ�����Li+��b���ƶ���A��ȷ��
B����ṹ�ĸ���﮽���������Ƚϴ�������﮽����ľ��ȳ������ѳ���B��ȷ��
C���ɷ�����֪�����ʱ����װ��Ϊ����װ�ã�b��Ϊ������������ӦΪ��LiFePO4-xe-= Li1-xFePO4+xLi+��C����
D���ɵ�ʧ�����غ�ͳ��ʱ�ĵ缫��Ӧ�ɵ����¹�ϵ��b������xmolLi+��b����������xmolLi+��xe-��a������xmolLi����ôb����������ֵ=a����������ֵ���ʵ�a����������mgʱ��������b����������mg��D��ȷ��
��ѡC��


 ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ���������ֵ������˵������ȷ���ǣ�������
A.���³�ѹ�£�32 g����������ԭ����ΪNA
B.��״���£�22.4 L ���Ȼ�̼�ķ�����ΪNA
C.0�棬101 kPa�£�44.8 L���������еķ�����Ϊ2NA
D.���³�ѹ�£�1 mol�������еķ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܵ�����������Ũ��ˮ��������ܵ��Ƿ�©����������Ӧ��8NH3+3Cl2=6NH4Cl+N2������������ȷ���ǣ� ��
A.NH3�ĵ���ʽΪ![]()
B.ÿת��3NA����ʱ������Cl2�����Ϊ33.6L
C.�ü�������й��ۼ������Ӽ��Ķ���������
D.�ø÷�������ܵ�й©�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(ij�������к�������[KAl(SO4)2��12H2O]��Al2O3��Fe2O3����һ���������ɼ�ʵ����ͼ��ʾ������֮���ת����

��ش��������⣺
��1��д��A��B�Ļ�ѧʽ��A___��B___��
��2���Լ�a���ѡ�������Լ��е���______��
A.NaOH��Һ B.ϡ���� C.������̼ D.��ˮ
д����Ӧ�����ӷ���ʽ___��
��3��д����Ӧ�ڣ�������ҺC�ͳ����������ӷ���ʽ___��
��4������D������Ϊ�����ԵĻ�ѧ���ϣ�D���������ʵĻ�ѧʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2����������[BrCH2CH2Br��������Ϊ��ɫҺ�壬������ˮ���ܶȱ�ˮ���۵�9�棬�е�132��]������Ѭ���������ܼ�����������ԭ������ʵ������ȡ��2C2H5OH![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br��
BrCH2CH2Br��
��֪��140��ʱ��������Ӧ��������(C2H5OC2H5)���ֲ����Ȼ�����SO2��CO2��
ʵ�鲽�����£�
�ٰ���ͼ��װ�������г�װ���ԣ�����������Ժ������Լ���
���ڱ�ˮԡ��ȴ�������£���20mLŨ���Ỻ���ӵ�10mL95%�Ҵ��У�ȡ��5mL���Һ����������ƿ�У���ʣ�ಿ�������ѹ��Һ©����
�ۼ���A��175�棬��ѹ��Һ©�������������μӻ��Һ��D��Һ�巴Ӧ��ȫ��
�ܽ�D�в����Ƶ���Һ©����������ˮ��NaOH��Һ��ˮϴ�Ӳ���Һ�����л����������MgSO4���壬���ˡ�����Y���ռ���BrCH2CH2Br4.23g��
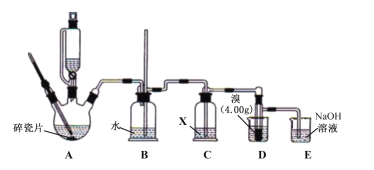
��ش��������⣺
��1��B�г����ܵ�������___��
��2���Լ�X��ѡ��___������ţ���
a.NaOH��Һ b.����NaHSO3��Һ c.���Ը��������Һ d.Ũ����
��3��D�о�֧�Թܻ����������ˮ��Ŀ����___����Ӧ������������ˮ��ȴ��֧�Թܣ�������ˮ���ɱ�ˮ������ǿ��ȴЧ��������Ҫȱ����___��
��4����������ƻ��Һʹ�õIJ�������������Ͳ������___��
��5����ֱ�ӽ�ȫ�����Һ���ȵ�170����ȣ����������175���������Һ�������μӻ��Һ������Ҫ���ŵ���___��
��6����Ӧ������E����Һ��BrO3-����E�з�����Ӧ�����ӷ���ʽΪ___��
��7������ܲ���YΪ___��
��8��BrCH2CH2Br�IJ���Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CO��H2�ڴ����������ºϳɼ״��������ķ�Ӧ���£�CO(g)+2H2(g)![]() CH3OH(g)�������һ�����ܱ������а����ʵ���֮��1��2����CO��H2�����ƽ��������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��ʾ������˵����ȷ����
CH3OH(g)�������һ�����ܱ������а����ʵ���֮��1��2����CO��H2�����ƽ��������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��ʾ������˵����ȷ����

A. �÷�Ӧ����H��0����p1��p2
B. ��Ӧ���ʣ�����(״̬A)������(״̬B)
C. ��C��ʱ��COת����Ϊ75%
D. �ں��º�ѹ���������ܱ������г��벻ͬ����CH3OH����ƽ��ʱCH3OH���������Ҳ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ס���(As)����(Sb)����(Bi)����(Mc)ΪԪ�����ڱ���ԭ���������������ͬ��Ԫ�ء��ش��������⣺
(1)����Ԫ�����ڱ��е�λ��______��![]() ��������Ϊ________��
��������Ϊ________��
��֪:P(s,����)=P(s,����) ��H=-39.3 kJ��mol-1��P(s,����)=P(s,����)����H=-17.6 kJ��mol-1���ɴ���֪,�������ȶ���������________��
(2)�������⻯�����ʵıȽϣ����ȶ���:NH3________PH3(����>������<��)���е㣺N2H4________P2H4(����>������<��)���ж�������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ľṹ��ʽ����![]() ����ʾ�����й��ڱ�����������ȷ����
����ʾ�����й��ڱ�����������ȷ����
A. ����Ҫ����ʯ��Ϊԭ�϶���õ�һ����Ҫ����ԭ��
B. ���к���̼̼˫�������Ա�����ϩ��
C. ��������6��̼̼��ѧ����ȫ��ͬ
D. ����������ˮ�����������Һ��Ӧ��ʹ������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50 mLϡH2SO4��ϡHNO3�Ļ����Һ���������ۣ�����������۵����������������������״����֮��Ĺ�ϵ��ͼ��ʾ����ÿһ��ֻ��Ӧһ����Ӧ������˵����ȷ���ǣ� ��
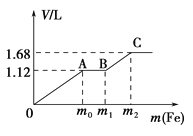
A. ��ʼʱ����������ΪH2
B. AB�η����ķ�ӦΪ�û���Ӧ
C. �μӷ�Ӧ���۵�������m2=5.6 g
D. ���û����Һ��c��HNO3��=0.5 molL��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com