
 ��
��| t/s | 0 | 500 | 1000 |
| c��N2O5��/mol•L-1 | 5.00 | 3.52 | 2.48 |
���� ��1������1����ԭ�ӱ�-NO2ȡ��������������
��2���ٺ��º����£���ͨ��һ������������Ӧ���������ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���
��500s��N2O5��Ũ�ȱ仯Ϊ��5-3.52��mol/L=1.48mol/L���ٸ���v=$\frac{��c}{��t}$����N2O5�ķֽ����ʣ�
����T2�¶ȸߣ���Ӧ���ʿ죬δ����ƽ��ʱ����ͬʱ����N2O5��Ũ�ȼ�С��������ӦΪ���ȷ�Ӧ������ƽ��ʱ�¶����ߣ�ƽ�������ƶ���N2O5��Ũ�Ȼ��С������T2�¶��£���Ӧ1000sʱ���NO2��Ũ��Ϊ4.98mol•L-1�����ʱN2O5��Ũ��Ϊ5mol/L-$\frac{1}{2}$��4.98mol•L-1=2.51mol/L��������T1�¶���1000sʱ���N2O5��Ũ�ȣ�˵��T2�¶��·�Ӧ���ʽ�����
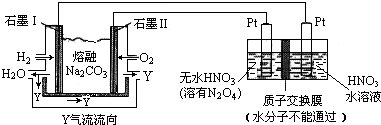
��3��ԭ��ظ�������������Ӧ����װ��ͼ��֪������������ʧȥ���ӣ���������̼������ӽ�����ɶ�����̼��ˮ����N2O4��ȡN2O5��Ҫ��ȥ���ӣ�����N2O5�����������ɣ�
��� �⣺��1���������Ľṹ��ʽ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2���ٺ��º����£�ͨ�뵪������Ӧ��������ֵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���N2O5��ת���ʲ��䣬
�ʴ�Ϊ�����䣻
���ɱ������ݿ�֪��500s��N2O5��Ũ�ȱ仯��Ϊ5mol/L-3.52mol/L=1.48mol/L����N2O5�ķֽ�����Ϊ$\frac{1.48mol/L}{500s}$=0.00296 mol•L-1•s-1��
�ʴ�Ϊ��0.00296 mol•L-1•s-1��
����T2�¶ȸߣ���Ӧ���ʿ죬δ����ƽ��ʱ����ͬʱ����N2O5��Ũ�ȼ�С��������ӦΪ���ȷ�Ӧ������ƽ��ʱ�¶����ߣ�ƽ�������ƶ���N2O5��Ũ�Ȼ��С������T2�¶��£���Ӧ1000sʱ���NO2��Ũ��Ϊ4.98mol•L-1�����ʱN2O5��Ũ��Ϊ5mol/L-$\frac{1}{2}$��4.98mol•L-1=2.51mol/L��������T1�¶���1000sʱ���N2O5��Ũ�ȣ�˵��T2�¶��·�Ӧ���ʽ��������¶�T2��T1��
�ʴ�Ϊ������
��3��ԭ��ظ�������������Ӧ����װ��ͼ��֪������������ʧȥ���ӣ���������̼������ӽ�����ɶ�����̼��ˮ�������缫��ӦʽΪ��H2+CO32--2e-�TH2O+CO2���ӵ��ԭ��������N2O4�Ʊ�N2O5Ϊ������Ӧ����N2O5Ӧ�����������ɣ�
�ʴ�Ϊ��H2+CO32--2e-�TH2O+CO2��������
���� ���⿼�黯ѧƽ�������Ӱ�����ء���ѧ��Ӧ���ʼ��㡢�绯ѧ��֪ʶ�㣬��2���Т�ѧ�������Ƿ�Ӧ�������⣬�����Ƿ���ƽ���ƶ����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.3g��������������Ӧ���������ʱ��ʧȥ�ĵ�����ĿΪ0.1NA | |
| B�� | 2.7g��������������������Һ��Ӧ������������������Ŀ��0.2NA | |
| C�� | 17gNH3������������ΪNA | |
| D�� | ��״���£�22.4L�����������������Ʒ�Ӧ��ת�Ƶ�����Ŀ��2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4V��A��=5V��B�� | B�� | 5V��B��=6VD | C�� | 2V��A��=3VD | D�� | 4V��B��=5VC |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��������ϸ��Ĥ�ڵ������ǣ�ϸ��Ĥ��ĸ���Һ�弰ϸ��Ĥ�����͵�����ԭ��أ������й��ж���ȷ���ǣ�������
��������ϸ��Ĥ�ڵ������ǣ�ϸ��Ĥ��ĸ���Һ�弰ϸ��Ĥ�����͵�����ԭ��أ������й��ж���ȷ���ǣ�������| A�� | �����ĵ缫��Ӧʽ������O2+4e-�T2O2- | |
| B�� | �����ĵ缫��Ӧʽ������O2+4e-+2H2O�T4OH- | |
| C�� | ������Ӧ��Ҫ��C6H12O6����CO2��HCO3- | |
| D�� | ������Ӧ��Ҫ��C6H12O6����CO2��HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4 HCl Mg��OH��2 MgCl2 | B�� | CO2 H2CO3 Na2CO3 Ca��HCO3��2 | ||
| C�� | H2O HNO3 NaOH KNO3 | D�� | SO3 NaHCO3 NaOH Na2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �������� | Cl- | CO32- | SO42- | NH4+ | Ba2+ |
| c/��mol•L-1�� | ��ȷ�� | 0.2 | 0.1 | 0.4 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com