
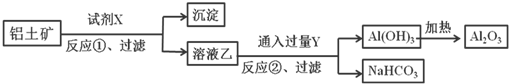
| A、反应①中试剂X是氢氧化钠溶液 |
| B、反应①、过滤后所得沉淀为氢氧化铁 |
| C、图中所示转化反应中包含一个氧化还原反应 |
| D、将试剂X和Y进行对换,最终可以达到相同的效果 |


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
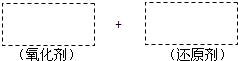
| A | C | |
| B |
| A、最高价氧化物对应水化物的酸性:C>B |
| B、C单质是氧化性最强的非金属单质 |
| C、A的氢化物中具有一定的还原性 |
| D、B在第三周期ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加入食盐 |
| Ⅰ |
| 通入足量气体B |
| Ⅱ |
| 过滤 |
| Ⅲ |
| Ⅳ |
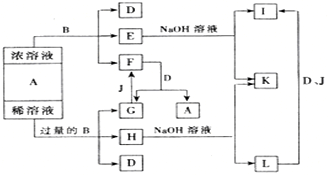
| A、A气体是NH3,B气体是CO2 |
| B、第Ⅲ步得到的晶体是发酵粉的主要成分 |
| C、第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
| D、第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10mL量筒量取7.13mL稀盐酸 |
| B、用酸式滴定管量取13.17mL稀盐酸 |
| C、用广泛pH试纸测得某溶液的pH为2.3 |
| D、用天平称取物品的质量为5.872g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容量 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2mol CH3OH | |
| 平衡时 数据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | α1 | α2 | α3 | |
| A、2c1>c3 |
| B、a+b<90.8 |
| C、2P2<P3 |
| D、α1+α3<1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com