
Į×ŌŚŃõĘųÖŠČ¼ÉÕ£¬æÉÄÜÉś³ÉĮ½ÖÖ¹ĢĢ¬Ńõ»ÆĪļ”£3£®1 gµÄµ„ÖŹĮ×£ØP£©ŌŚ3£®2 g µÄŃõĘųÖŠČ¼ÉÕ£¬ÖĮ·“Ó¦Īļŗľ”£¬²¢·Å³öX kJČČĮ攣
£Ø1£©Ķعż¼ĘĖćČ·¶Ø·“Ó¦²śĪļµÄ×é³É£ØÓĆ»ÆѧŹ½±ķŹ¾£©ŹĒ______________£¬ĘäĻąÓ¦µÄÖŹĮæĪŖ________”£
£Ø2£©ŅŃÖŖµ„ÖŹĮ×µÄČ¼ÉÕČČĪŖY kJ”¤mol-1£¬Ōņ1 mol PÓėO2·“Ӧɜ³É¹ĢĢ¬P2O3µÄ·“Ó¦ČȦ¤H=________”£
£Ø3£©Š“³ö1 mol PÓėO2·“Ӧɜ³É¹ĢĢ¬P2O3µÄČČ»Æѧ·½³ĢŹ½£ŗ________________”£
ĆüĢāŅāĶ¼£ŗ±¾ĢāŅŌĮ×ĪŖŌŲĢ壬漲éČ¼ÉÕČČ”¢øĒĖ¹¶ØĀɼ°ČČ»Æѧ·½³ĢŹ½µÄÓŠ¹ŲÖŖŹ¶£¬ÖŲµćŹĒæ¼²éČ¼ÉÕČȶØŅåŗĶøĒĖ¹¶ØĀɵĥķ½āŗĶÓ¦ÓĆ£¬¶ųÉę¼°Į×µÄÖŖŹ¶²¢²»ø“ŌÓ”£
(1)P2O3ŗĶP2O5 2£®75 gŗĶ3£®55 g
(2)-(20X-Y) kJ”¤mol-1
(3)P(s)+![]() O2(g)====
O2(g)====![]() P2O3(s)£»¦¤H=-(20X-Y) kJ”¤mol-1
P2O3(s)£»¦¤H=-(20X-Y) kJ”¤mol-1
£Ø1£©ÓÉĢāŅāµĆÉś³ÉµÄĮ½ÖÖŃõ»ÆĪļ·Ö±šĪŖP2O3ŗĶP2O5£¬ÉčÉś³ÉP2O3ŗĶP2O5ŠčPµÄĪļÖŹµÄĮæ·Ö±šĪŖx”¢y£¬øł¾Ż·“Ó¦·½³ĢŹ½£ŗ4P+3O2====2P2O3ŗĶ4P+5O2====2P2O5µĆ
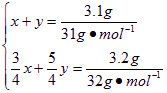
½āµĆx=y=0£®05 mol”£
£Ø2£©ÓÉČ¼ÉÕČȵĶØŅ壬ĶĘ³ö0£®05 molĮ×µ„ÖŹĶźČ«Č¼ÉշųöµÄČČĮæĪŖ0£®05 Y kJ£¬ŌņÉś³ÉP2O3Ź±·Å³öµÄČČĮæĪŖ£ØX-0£®05Y£©kJ£¬“Ó¶ųĶĘ³ö1 molĮ×µ„ÖŹČ¼ÉÕÉś³ÉP2O3Ź±·Å³öµÄČČĮæĪŖ![]() (X-0£®05Y)kJ£¬¼“£Ø20X-Y£©kJ”£
(X-0£®05Y)kJ£¬¼“£Ø20X-Y£©kJ”£


 »„¶ÆÓ¢ÓļĻµĮŠ“š°ø
»„¶ÆÓ¢ÓļĻµĮŠ“š°ø ĆūÅĘѧŠ£·Ö²ćÖÜÖܲāĻµĮŠ“š°ø
ĆūÅĘѧŠ£·Ö²ćÖÜÖܲāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 3 |
| 4 |
| 1 |
| 2 |
| 3 |
| 4 |
| 1 |
| 2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 3 |
| 4 |
| 1 |
| 2 |
| 3 |
| 4 |
| 1 |
| 2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
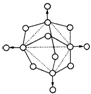 Į×ŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕ£¬Éś³ÉXµÄ·Ö×Ó½į¹¹ČēÓŅĶ¼ĖłŹ¾£®Ķ¼ÖŠŹµĻß±ķŹ¾»Æѧ¼ü£¬Ō²Č¦±ķŹ¾Ō×ӣز»æ¼ĀĒŌ×ÓĢå»ż“󊔣©
Į×ŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕ£¬Éś³ÉXµÄ·Ö×Ó½į¹¹ČēÓŅĶ¼ĖłŹ¾£®Ķ¼ÖŠŹµĻß±ķŹ¾»Æѧ¼ü£¬Ō²Č¦±ķŹ¾Ō×ӣز»æ¼ĀĒŌ×ÓĢå»ż“󊔣©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
(1)Ķعż¼ĘĖćČ·¶Ø·“Ó¦²śĪļµÄ×é³É(ÓĆ»ÆѧŹ½±ķŹ¾)ŹĒ________£¬ĘäĻąÓ¦µÄÖŹĮæ(g)ĪŖ_______”£
(2)ŅŃÖŖµ„ÖŹĮ×µÄČ¼ÉÕČČĪŖY kJ”¤mol-1£¬Ōņ1 mol PÓėO2·“Ӧɜ³É¹ĢĢ¬P2O3µÄ·“Ó¦ČȦ¤H=______”£
(3)Š“³ö1 mol PÓėO2·“Ӧɜ³É¹ĢĢ¬P2O3µÄČČ»Æѧ·½³ĢŹ½£ŗ___________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø1£©Ķعż¼ĘĖćČ·¶Ø·“Ó¦²śĪļµÄ×é³É£ØÓĆ»ÆѧŹ½±ķŹ¾£©ŹĒ £¬ĘäĻąÓ¦µÄÖŹĮæ£Øg£©ĪŖ ”£
£Ø2£©ŅŃÖŖµ„ÖŹĮ×µÄČ¼ÉÕČČĪŖY kJ/mol£¬Ōņ1mol PÓėO2·“Ӧɜ³É¹ĢĢ¬P2O3µÄ·“Ó¦ČȦ¤H£½ ”£
£Ø3£©Š“³ö1mol PÓėO2·“Ӧɜ³É¹ĢĢ¬P2O3µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com