
分析 (1)O2和O3的构成原子都是氧原子,所以等质量的O2和O3所以含原子数目相等;
(2)①根据n=c•V和m=n•M来计算;
②根据1molNa2CO3•10H2O能提供1molNa2CO3,得出需要的Na2CO3•10H2O的物质的量,再根据m=n•M来计算质量;
③根据稀释定律C浓V浓=C稀V稀来计算;
④根据C=$\frac{1000ρω}{M}$计算出溶液的浓度,然后根据稀释定律C浓V浓=C稀V稀来计算;
(3)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析,凡是不当操作使n偏小或者使V偏大的操作都会使溶液浓度偏低,凡是不当操作使n偏大或者使V偏小的操作都会使溶液浓度偏高,据此解答.
解答 解:(1)O2和O3的构成原子都是氧原子,所以等质量的O2和O3所以含原子数目相等,则96克的O2和O3的气体混合,其氧原子个数为1;1,故答案为:1:1;
(2)①根据n=c•V可知需要的Na2CO3的物质的量n=1mol•L-1×0.25L=0.25mol,质量m=n•M=0.25mol×106g/mol=26.5g,
故答案为:26.5;
②根据1molNa2CO3•10H2O能提供1molNa2CO3,可知需要的Na2CO3•10H2O的物质的量n=0.25mol,根据m=n•M=0.25mol×286g/mol=71.5g,
故答案为:71.5;
③设物质的量浓度为4mol•L-1的Na2CO3溶液Xml,根据稀释定律C浓V浓=C稀V稀可知:4mol/L×Xml×10-3=1mol/L×0.25L,解得X=62.5ml,
故答案为:62.5;
④根据C=$\frac{1000ρω}{M}$可知质量分数为12%、密度为1.12g•cm-3的Na2CO3溶液的C=$\frac{1000×1.12×12%}{106g/mol}$=1.27mol/L,设需要此Na2CO3溶液的体积为Xml,则根据稀释定律C浓V浓=C稀V稀可知:1.27mol/L×Xml×10-3=1mol/L×0.25L,解得X=196.85ml,
故答案为:196.85;
(3)A.固体Na2CO3•10 H2O放在右盘,则称量时,药品的实际质量偏小,所以配制的溶液的浓度偏小,故A选;
B.容量瓶用碳酸钠溶液先润洗,容量瓶中碳酸钠的物质的量偏大,所以配制的溶液的浓度偏大,故B不选;
C.转移溶液时未洗涤烧杯,烧杯中有残留的碳酸钠,则容量瓶中碳酸钠的物质的量偏小,所以配制的溶液的浓度偏小,故C选;
D.定容时,溶液未冷却,冷却后溶液的体积减小,所以配制的溶液的浓度偏大,故D不选;
E.定容时视线仰视,溶液的体积偏大,则配制的溶液的浓度偏小,故E选;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水,溶液的浓度不变,故F不选;
G.容量瓶未干燥,对溶液的体积无影响,溶液的浓度不变,故G不选;
故选ACE.
点评 本题考查了物质的量的计算、一定物质的量浓度溶液的配制过程中的计算和误差分析,准确判断不当操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.


 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl-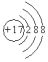 | B. | Cl- 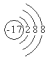 | C. | Cl+ 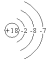 | D. | Cl+ 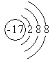 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
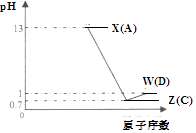
| A. | A的离子半径小于B的离子半径 | |
| B. | W、X两物质含有的化学键类型相同 | |
| C. | B的简单离子会影响水的电离平衡 | |
| D. | D的氢化物稳定性大于C的氢化物稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酒越陈越香与酯化反应有关 | |
| B. | 乙烷、丙烷和丁烷都没有同分异构体 | |
| C. | 乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与足量氯气在光照下反应可生成难溶于水的油状液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 熔点:已烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 含氢量:甲烷>乙烷>乙烯>乙炔>苯 | |
| C. | 密度:CCl4>H2O>苯 | |
| D. | 相同物质的量物质完全燃烧耗O2量:已烷>环已烷>苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
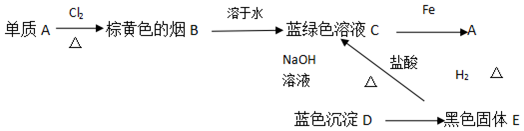
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糯米酿制甜酒的过程中,有部分淀粉转化为乙醇 | |
| B. | “滴水石穿、绳锯木断”都涉及化学变化 | |
| C. | 亚硝酸钠易致癌,但火腿肠中允许含少量的亚硝酸钠以保持肉质新鲜 | |
| D. | 大量燃烧化石燃料排放的废气中含SO2,造成大气污染,使雨水pH<5.6形成酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含分子数之比为1:1:1 | B. | 所含氢原子数之比为4:2:3 | ||
| C. | 质量之比为16:18:17 | D. | 摩尔质量之比为1:1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com