
��12�֣�830Kʱ�����ܱ������з������п��淴Ӧ��CO��g��+H2O��g��![]() CO2��g��+H2��g�� ��H��0�����Իش��������⣺
CO2��g��+H2��g�� ��H��0�����Իش��������⣺
��1������ʼʱc��CO��=2 mol��L-1��c��H2O��=3 mol��L-1���ﵽƽ��ʱCO��ת����Ϊ60%�����ڸ��¶��£��÷�Ӧ��ƽ�ⳣ��K= ���� .
��2������ͬ�¶��£�����ʼʱc��CO��=1 mol��L-1��c��H2O��=2 mol��L-1����Ӧ����һ��ʱ����H2��Ũ��Ϊ0.5 mol��L-1�����ʱ�÷�Ӧ�Ƿ�ﵽƽ��״̬ ����ǡ��롰������ʱv������ v���棩������ڡ���С�ڡ����ڡ��������жϵ�������
��������
��3���������¶ȣ��÷�Ӧ��Kֵ�� ���÷�Ӧ�Ļ�ѧ��Ӧ���ʽ� �� �����������С�����䡱����
��1��1 ��2������ ��Ϊ��ʱ��С��ƽ�ⳣ��1����������Ӧ���ʴ����淴Ӧ���ʡ�
��3������ ��С
����:������淴Ӧ���йؼ��㼰��������Է�Ӧ���ʺ�ƽ�ⳣ����Ӱ�졣
��1�� CO��g��+H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼŨ�ȣ�mol/L�� 2 3 0 0
ת����Ũ�ȣ�mol/L�� 1.2 1.2 1.2 1.2
ƽ��Ũ�ȣ�mol/L�� 0.8 1.8 1.2 1.2
����ƽ�ⳣ���ı���ʽ��֪K��
��2�� CO��g��+H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼŨ�ȣ�mol/L�� 1 2 0 0
ת����Ũ�ȣ�mol/L�� 0.5 0.5 0.5 0.5
ijʱ��Ũ�ȣ�mol/L�� 0.5 1.5 0.5 0.5
��ʱ��1
����û�дﵽƽ��״̬����ʱ����Ӧ���ʴ����淴Ӧ���ʡ�
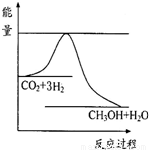
��3����Ϊ��Ӧ�Ƿ��ȷ�Ӧ�����Խ����¶ȣ�ƽ��������Ӧ�����ƶ������ƽ�ⳣ�������¶ȷ�Ӧ���ʼ�С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2009-2010ѧ��ɽ��ʡ̩���зʳ�һ�и������ϣ���ĩ��ѧ�ۺ�ѵ����һ���������棩 ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com