
分析 (1)根据判断平衡状态的方法:V正=V逆,各组分的浓度保持不变则说明已达平衡,据此进行判断;
(2)根据Ksp=c(Cr3+)•c3(OH-)来计算氢氧根离子离子的浓度,并计算氢离子浓度和pH的大小.
解答 解:(1)a.Cr2O72-和CrO42-的浓度相同取决于起始浓度和转化浓度,无法判断各组分的浓度是否变化,则不能判断平衡状态,故a错误;
b.2v(Cr2O72-)=v(CrO42-),无法判断正逆反应速率关系,则不能判断平衡状态,故b错误;
c.溶液的颜色不变,说明各组分的浓度不再变化,能够判断该反应达到平衡状态,故c正确;
故答案为:c;
(2)Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,则需c(OH-)=$\root{3}{\frac{{K}_{sp}}{c(C{r}^{3+})}}$=$\root{3}{\frac{1×1{0}^{-32}}{1×1{0}^{-5}}}$=10-9mol/L,所以c(H+)=$\frac{1×1{0}^{-14}}{1×1{0}^{-9}}$mol/L=10-5mol/L,该溶液的pH=5,
故答案为:5.
点评 本题考查难溶物溶解平衡的计算、化学平衡状态的判断,题目难度中等,明确化学平衡及其影响为解答关键,注意掌握溶度积的表达式及计算方法,试题培养了学生的分析能力及化学计算能力.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属氧化物都是碱性氧化物 | |
| B. | 氨水和液氯都是纯净物 | |
| C. | CuSO4溶液和Al(OH)3胶体都能产生丁达尔效应 | |
| D. | 碳酸氢钠属于盐类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,将22.4L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA | |
| B. | 常温常压下,16gCH4所含中子数目为8NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA | |
| D. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A组 | B组 | C组 | D组 | |
| 分类标准 | 碱 | 常温下为固体 | 金属单质 | 酸 |
| 不属于该类别的物质 | SO2 | Cl2 | H2 | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
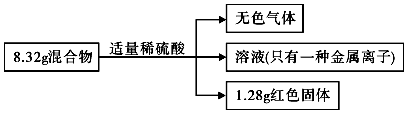
| A. | 无色气体的体积为2.24L | |
| B. | 原混合物中铁的质量为6.72g | |
| C. | 反应后的溶液中金属离子物质的量为0.02 mol | |
| D. | 反应消耗的H2SO4物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气、硫酸铜、硫酸 | B. | 乙酸、空气、纯碱 | ||
| C. | 氧化铁、胆矾、熟石灰 | D. | 硝酸、蔗糖水、氢氧化铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2、NaHSO4 | B. | Na2CO3、HNO3 | C. | NaHCO3、AlCl3 | D. | NaOH、CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制金属钠:电解饱和食盐水 | |
| B. | 工业炼铁:需要用到的原料有铁矿石、一氧化碳、空气和石灰石 | |
| C. | 冶炼镁:将六水合氯化镁晶体在一定条件下加热得到无水氯化镁,电解熔融氯化镁,可以得到金属镁 | |
| D. | 生物炼铜法:利用某种能耐受铜盐毒性的细菌,这种细菌利用空气中的填氧气氧化硫化铜矿石,把不溶性的硫化铜直接转化为单质铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
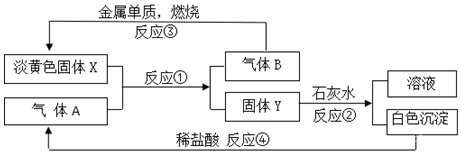
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com