
 右图
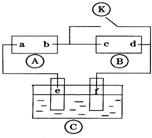
右图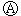 为直流电源,
为直流电源,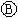 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,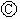 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现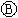 上的c点显红色.为实现铁上镀铜,接通
上的c点显红色.为实现铁上镀铜,接通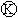 后,使c.d两点短路.下列叙述正确的是( )
后,使c.d两点短路.下列叙述正确的是( )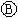 上的c点显红色判断c的电极,根据c的电极判断a、b的电极并判断e、f的电极,再根据阴阳极上发生的反应写出相应的电极反应,判断反应类型,然后根据溶液中离子的放电情况结合生成物反应物写出相应的方程式.
上的c点显红色判断c的电极,根据c的电极判断a、b的电极并判断e、f的电极,再根据阴阳极上发生的反应写出相应的电极反应,判断反应类型,然后根据溶液中离子的放电情况结合生成物反应物写出相应的方程式.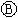 外接电源,所以
外接电源,所以 是电解氯化钠溶液的电解池,
是电解氯化钠溶液的电解池, 上的c点显红色,说明c点有氢氧根离子生成,根据离子的放电顺序知,该极上氢离子得电子放电,所以c是阴极,外电源b是负极,a是正极,故A错误;
上的c点显红色,说明c点有氢氧根离子生成,根据离子的放电顺序知,该极上氢离子得电子放电,所以c是阴极,外电源b是负极,a是正极,故A错误;

科目:高中化学 来源:2013-2014学年山东省烟台市高三上学期期末统考化学试卷(解析版) 题型:填空题
某蓄电池反应为NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。
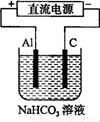
(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:

已知:
|
沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
|
开始沉淀时的pH |
2.3 |
7.5 |
5.6 |
6.2 |
|
完全沉淀时的pH |
3.9 |
9.7 |
6.4 |
8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com