
 ;
;分析 (1)根据n=$\frac{m}{M}$计算有机物A、二氧化碳、水的物质的量,根据原子守恒计算烃分子中C、H原子数目,根据相对原子质量计算分子中氧原子数目,据此书写该烃的分子式;
(2)红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1,分子中有3种不同的H原子,原子数目之比为6:1:1,结合有机物的分子式判断有机物A的结构;
(3)根据有机物A含有是官能团进行分析解答.
解答 解:(1)有机物A只含有C、H、O三种元素,质谱图表明其相对分子质量为84,16.8g有机物A的物质的量=$\frac{16.8g}{84g/mol}$=0.2mol,经燃烧生成44.0g CO2,物质的量为1mol,生成14.4g H2O,物质的量为$\frac{14.4g}{44g/mol}$=0.8mol,故有机物A分子中N(C)=$\frac{1mol×1}{0.2mol}$=5,N(H)=$\frac{0.8mol×2}{0.2mol}$=8,故N(O)=$\frac{84-12×5-8}{16}$=1,故A的分子式为C5H8O,
故答案为:C5H8O;
(2)不饱和度为:$\frac{2×5+2-8}{2}$=2,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1,故分子中含有2个CH3、1个-OH连接在同一C原子上,所以A的结构简式为: ,
,
故答案为: ;
;
(3)红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,不饱和度为$\frac{2×5+2-8}{2}$=2,不含其它官能团,含有羟基,能与钠反应,含有C≡C双键,能与Na发生取代反应,能与溴发生加成反应,能与氢气发生加成反应,
故答案为:ABC.
点评 本题考查有机物的推断,涉及分子式、结构式的确定、官能团性质、同分异构体书写等知识,题目难度中等,是对学生综合能力的考查,确定分子式是解题的关键,注意掌握常见有机物结构与性质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①②③④⑤ | C. | ①②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素和非金属分界线附近的元素 | |
| B. | 左、下方区域的金属元素 | |
| C. | 右、上方区域的非金属元素 | |
| D. | 稀有气体元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地沟油经过处理,可用来制造肥皂 | |
| B. | 向食品中添加抗氧化剂(维C)可以对食物起到防腐作用 | |
| C. | 我国的汽油标准已由“国Ⅲ”提高到国“Ⅳ”,这意味着汽车不再排放氮氧化合物 | |
| D. | CO2和CH4都是产生温室效应的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
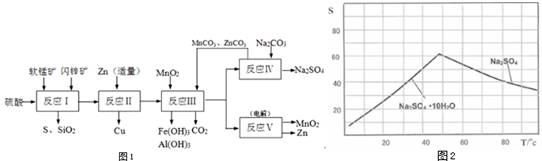
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
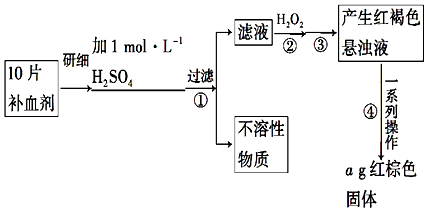
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
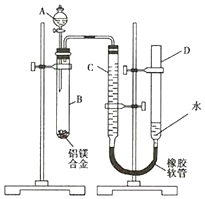 某学习小组用如图装置测定镁铝合金中铝的质量分数.
某学习小组用如图装置测定镁铝合金中铝的质量分数.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Zn | A | B | C | D |
| 正极 | Fe | C(石墨) | Ag | Zn |
| 负极 | Cu | Fe | Fe | Fe |
| 电解质溶液 | FeCl3 | Fe2 (SO4)3 | H2SO4 | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com