
【题目】含铬化合物的废水有毒,特别是Cr(Ⅵ)有致癌作用,对农作物及微生物的毒害很大.目前处理的方法较多,还原沉淀法是较为广泛的处理含铬废水的方法,流程如图: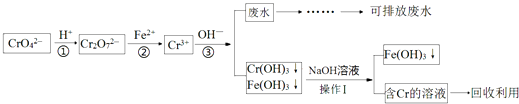
(1)步骤①中存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O该反应的平衡常数表达式K=;碱性溶液中Cr(Ⅵ)离子的颜色呈 . (填“黄色”或“橙色”)
(2)上述操作Ⅰ的名称为 , 以下物质可用于代替步骤②中的Fe2+的是
A.KMnO4(H+) B.HNO3 C.Na2SO3
(3)步骤③中出水总铬与溶液的pH关系如图,下列说法不正确的是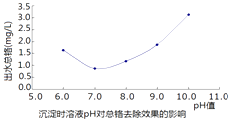
A.为有效除去Cr3+ , 加入的碱越多越好
B.Cr(OH)3可溶于强碱
C.要除去Cr3+ , 调节pH值最好为7左右
(4)已知Ksp[Cr(OH)3]=1.1×10﹣32 , 按《污水综合排放标准》,水质中总铬的浓度应小于3×10﹣5molL﹣1 , 当步骤③调节pH=6时,该处理后的污水是否达到排放标准?(填“是”或“否”).
【答案】
(1)![]() ;黄色
;黄色
(2)过滤;C
(3)A
(4)是
【解析】解:在酸性条件下CrO42﹣转化为Cr2O72﹣ , 加入铁粉,发生氧化还原反应生成Cr3+ , 加入碱生成Cr(OH)3、Fe(OH)3 , Cr(OH)3可溶于强碱,加入过量氢氧化钠,Cr(OH)3溶解,然后过滤,经滤液进行会后利用.
(1.)反应2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O化学平衡常数K= ![]() ,碱性溶液中平衡逆向移动,溶液呈黄色,
,碱性溶液中平衡逆向移动,溶液呈黄色,
所以答案是: ![]() ;黄色;
;黄色;
(2.)操作Ⅰ用于分离固体和液体,为过滤操作,步骤②中的Fe2+表现出还原性,可用Na2SO3替代,所以答案是:过滤; C;
(3.)与流程信息可知Cr(OH)3可溶于强碱,则碱不能加入过多,由图象可知要除去Cr3+ , 调节pH值最好为7左右,所以答案是:A;
(4.)已知Ksp[Cr(OH)3]=1.1×10﹣32 , 水质中总铬的浓度应小于3×10﹣5molL﹣1 , 当步骤③调节pH=6时,c(OH﹣)=1×10﹣8molL﹣1 , 则c(Cr3+)= ![]() mol/L<3×10﹣5molL﹣1 , 达到排放标准,
mol/L<3×10﹣5molL﹣1 , 达到排放标准,
所以答案是:是.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】室温下,有pH均为9体积均为10mL的NaOH溶液和CH3COONa溶液,下列说法正确的是( )
A.两种溶液中的c(Na+)相等
B.两溶液中由水电离出的c(OH﹣)之比为 ![]()
C.分别加水稀释到100mL时,两种溶液的pH依然相等
D.分别与同浓度的盐酸反应,恰好反应时消耗的盐酸体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用右图装置探究铁在海水中的电化学防护,下列说法不正确的是( ) 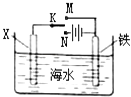
A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀
B.若X为锌棒,开关K置于M处,铁电极的反应:Fe﹣2e﹣→Fe2+
C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀
D.若X为碳棒,开关K置于N处,铁电极的反应:2H++2e﹣→H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应N2O4(g)2NO2(g)△H=+57kJmol﹣1 , 在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( ) 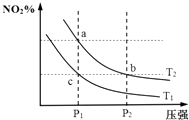
A.反应温度:T1>T2
B.a、b两点的平衡常数:Kb>Ka
C.a、c两点气体的颜色:a浅,c深
D.b、c两点的反应速率:v(b)>v(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.植物油氢化过程发生了加成反应B.淀粉和纤维素互为同分异构体
C.环己醚与苯可用酸性KMnO4溶液鉴别D.水可以用来分离溴苯和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m1g铜铝合金投入到1 L含H2SO4和HNO3的混合溶液中,合金完全溶解后只生成VL —氧化氮气体(标准状况),向反应后的溶液中逐滴加入1mol/L NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积的关系如下图所示。下列说法中不正确的是:
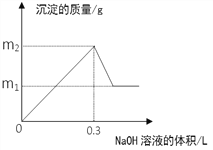
A. 2c(H2SO4) + c(HNO3) = 0.8 mol·L-1
B. m2—m1=5.1
C. 原合金中铝的质量分数为34.7%
D. V = 2.24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中c(H+)与c(OH﹣)有如图所示关系,下列有关说法正确的是( ) 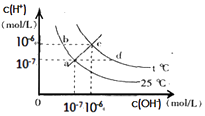
A.c点对应的溶液中大量存在的离子可能为:Na+、H+、Cl﹣、NO3﹣
B.将25℃时的KCl溶液加热到t℃,则该溶液中的c(OH﹣)由a点变化到b点
C.t℃<25℃
D.ac线上的任意一点溶液均有c(H+)=c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是( )
A. 100mL12mol/L浓盐酸与足量的MnO2加热充分反应生成Cl2分子数为0. 3 NA
B. 80gSO3在标准状况下所占体积约为22.4L
C. 向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,转移的电子的数目为NA
D. 5.4g铝粉与足量的氢氧化钠溶液充分反应生成H2分子数为0. 3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com