
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| B. | 氨水中通入过量SO2:NH3•H2O+SO2═HSO3-+NH4+ | |
| C. | 饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
分析 A.硫酸根离子恰好沉淀时,硫酸铝铵与氢氧化钡按照物质的量1:2反应,铵根离子结合氢氧根离子能力大于氢氧化铝,反应生成氢氧化铝沉淀和一水合氨;
B.二氧化硫过量,反应生成亚硫酸氢铵;
C.两溶液反应生成碳酸钙沉淀、氢氧化钠和水;
D.氢离子、氢氧根离子的系数不满足硫酸、氢氧化钙的化学式组成.
解答 解:A.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,反应生成氢氧化铝、硫酸钡沉淀和一水合氨,反应的离子方程式为:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓,故A正确;
B.氨水中通入过量SO2,反应生成亚硫酸氢铵,反应的离子方程式为:NH3•H2O+SO2═HSO3-+NH4+,故B正确;
C.饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液,反应生成NaOH、碳酸钙沉淀和水,反应的离子方程式为:Ca2++HCO3-+OH-═CaCO3↓+H2O,故C正确;
D.氢氧化钙溶液与等物质的量的稀硫酸混合,反应生成微溶物硫酸钙和水,正确的离子方程式为:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O,故D错误;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:填空题
| 被鉴别的物质 | 鉴别物质(或鉴别方法) | 现象(填入序号即可) |
| 葡萄糖 | 新制氢氧化铜 | ④ |
| 淀粉 | 碘水 | ② |
| 蛋白质 | 浓硝酸 | ⑤ |
| 蛋白质 | 燃烧 | ① |
| 葡萄糖 | 银氨溶液 | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积:④>①>②>③ | B. | 密度:②>③>①>④ | ||
| C. | 质量:②>③>①>④ | D. | 氢原子数:①>②>③>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度 | B. | 混合气体的压强 | ||
| C. | 混合气体的平均摩尔质量 | D. | SO2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 1mol/L NaCl 溶液 | B. | 75mL 2mol/L CaCl2溶液 | ||
| C. | 150mL 2mol/L KCl 溶液 | D. | 75mL 1mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
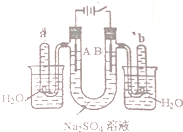 如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( )
如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( )| A. | 逸出气体的体积,A电极的小于B电极的 | |
| B. | 一电极逸出无味气体,另一电极逸出刺激性气味气体 | |
| C. | A电极附近呈红色,B电极附近呈蓝色 | |
| D. | 电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶解呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
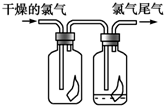 (1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+1s22s22p63s23p6 | B. | O2-1s22s22p4 | ||
| C. | Cl- 1s22s22p63s23p6 | D. | Ar1s22s22p63s23p6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com