
 4Na[Au(CN)2]+4NaOH;
4Na[Au(CN)2]+4NaOH; 2Au+Na2[Zn(CN)4]。
2Au+Na2[Zn(CN)4]。| A.Na[Au(CN)2]不溶于水 |
| B.化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C.金元素在地壳中能以化合态的形式存在 |
| D.在提炼过程中含金元素的物质始终作氧化剂 |
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源:不详 题型:多选题
| A.NH4+ | B.Fe2+ | C.Mg2+ | D.Al3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含金属元素的离子不一定都是阳离子 |
| B.在氧化还原反应中,非金属单质一定是氧化剂 |
| C.某元素从化合态变为游离态时,该元素一定被还原 |
| D.金属阳离子被还原不一定得到金属单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.羟甲基(-CH2OH)和甲氧基(CH3O-)电子数不相等 |
B.S2-的结构示意图: |
C.苯甲醛: |
D.质子数为53,中子数为78的碘原子: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.甲基的电子式: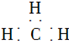 |
B.镁离子的结构示意图: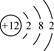 |
C.质量数为34、中子数为18的核素: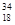 S S |
D.乙酸的结构简式: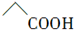 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.硝基苯的结构简式: | B.乙醇含有的官能团是—OH,带一个单位负电荷 |
C.丙烷的球棍模型为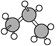 | D.乙酸的分子式:C2H4O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
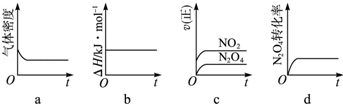
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.6.4 g铜粉与足量硫粉充分反应,失去的电子数为0.2 NA |
| B.Na2O2与足量H2O反应生成0.2molO2,转移电子的数目为0.4 NA |
| C.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2 NA |
| D.0.5 mol·L-1CuCl2溶液中含有Cu2+数小于0.5 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
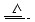 CuSO4+A↑+2H2O
CuSO4+A↑+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com