
A、 如图装置可测定反应速率 |
| B、配制FeCl2溶液时,需加入少量铁粉和稀盐酸 |
| C、用碱式滴定管盛装KMnO4溶液滴定FeSO4溶液 |
| D、分别加热蒸干灼烧NaAlO2溶液和AlCl3溶液,最终都能得到Al2O3 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时电解质溶液显强酸性 |
| B、充电时阳板反应为Ni(OH)2+2OH--2e-=NiO2+2H2O |
| C、放电时正极附近溶液pH减小 |
| D、充电时阴极附近溶液的碱性保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大量排放SO2是造成温室效应的主要原因 |
| B、明矾和硫酸铁都常用于净水 |
| C、考古时常用14C测定文物的年代 |
D、 如图是运输浓硝酸的槽罐车上贴的危险警告标签 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、对应简单离子半径:X>W |
| B、对应气态氢化物的稳定性Y>Z |
| C、化合物XZW既含离子键,又含共价键 |
| D、Y的氧化物能与Z的氢化物和X的最高价氧化物对应的水化物的溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
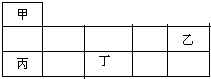 短周期金属元素甲~丁在元素周期表中的相对位置如图所示:下列判断正确的是( )
短周期金属元素甲~丁在元素周期表中的相对位置如图所示:下列判断正确的是( )| A、原子半径:丙>丁>乙 |
| B、单质的还原性:丁>丙>甲 |
| C、甲、乙、丙的氧化物均为共价化合物 |
| D、乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaNO3、NH3?H2O、N2 |
| B、Fe、CH3COOH、液氯 |
| C、漂白粉、BaSO4、CO2 |
| D、Ba(OH)2、HF、酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com