
【题目】乙醇是一种重要的化工原料,由乙醇衍生出的部分化工产品如图所示:

回答下列问题:
(1)C中含有的官能团名称是__________.
(2)E是一种常见的塑料,其化学名称是__________.
(3)由乙醇生产F的化学反应类型为__________.
(4)由乙醇生成G的化学方程式为__________.
(5)写出由A生成B的化学方程式:__________.
【答案】羟基、氯原子 .聚氯乙烯 消去反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3CH2OH+CH3COOH
2CH3CHO+2H2O CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
【解析】
(1)乙醇与氯气发生取代反应生成ClCH2CH2OH,C中含有的官能团名称是羟基、氯原子;
(2)ClCH2CH2OH在浓硫酸作用下发生消去反应生成氯乙烯,聚合生成E,E是一种常见的塑料,其化学名称是聚氯乙烯.
(3)CH3CH2OH在浓硫酸作用下发生消去反应生成F乙烯,由乙醇生产F的化学反应类型为消去反应.
(4)乙醇在铜作催化剂和氧气作用下氧化生成乙醛,化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O.
2CH3CHO+2H2O.
(5)CH3COOH和CH3CH2OH在浓硫酸、加热条件下生成B:CH3COOCH2CH3,化学方程式:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。


科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。试回答:

(1)若X是强氧化性单质,则A不可能是____。
a.S b.N2 c.Na d.Mg e.Al
(2)若A为强碱溶液,则X可能为____。
a.CO2 b.AlCl3 c.Al d.Mg e.Al2O3
(3)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为____;C溶液在贮存时应加入少量X,理由是(离子方程式表示)___,检验此C溶液中金属元素价态的操作方法是____。
(4)若A、B、C为含有金属元素的化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为____,X的化学式可能为(写出不同类物质)____或____,反应②的离子方程式为___或___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A物质在一定条件下可转化为其它物质,已知A分子中所有碳原子不在同一条直线上,根据图示填空:

(1)化合物A含有的官能团名称是__。
(2)A转化为E的化学方程式是___。
(3)与A具有相同官能团的A的同分异构体的结构简式是__。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是__。
(5)F的结构简式是__,由E生成F的反应类型是__,由B生成D的反应类型是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收废水中苯酚的过程如图所示。下列分析错误的是
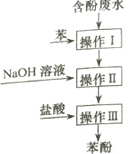
A. 操作I中苯作萃取剂
B. 苯酚钠在苯中的溶解度比在水中的大
C. 通过操作II苯可循环使用
D. 三步操作均需要分液漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用菱镁矿(主要含MgCO3,FeCO3杂质)制取碱式氯化镁[Mg(OH)Cl]的流程。已知:MgO用于调节沉淀池中溶液的pH值。

金属离子 | pH | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Mg2+ | 8.8 | 11.4 |
下列说法不正确的是( )
A.酸浸池中加入的![]() 酸可以是硫酸
酸可以是硫酸
B.加入MgO后的沉淀一定含有Fe(OH)3
C.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
D.制得碱式氯化镁的方程式为:MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑
Mg(OH)Cl+HCl↑+5H2O↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家艾哈迈德·泽维尔使“运用激光技术观察化学反应时分子中原子的运动”成为可能,在他的研究中证实了光可诱发下列变化:这一事实可用于解释人眼的夜视功能,有关X、Y的叙述不正确的是( )
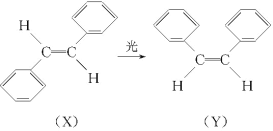
A.X和Y互为同分异构体
B.X和Y发生聚合反应生成的高分子化合物为纯净物
C.X和Y都可发生加聚反应
D.X和Y分子中所有原子可以处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
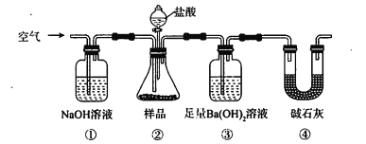
下列说法不正确的是
A. 必须在②③间添加吸收HCl的装置
B. ④的作用是防止空气中的气体影响实验的精确度
C. 通入空气的作用是保证②中产生的气体完全转移到③中
D. 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:10NaN3+2KNO3═K2O+5Na2O+16N2↑,则下列说法正确的是( )
A.KNO3是氧化剂,KNO3中N元素被氧化
B.生成物中的Na2O是氧化产物,K2O是还原产物
C.每转移1mole﹣,可生成标准状况下N2的体积为35.84升
D.若有65gNaN3参加反应,则被氧化的N的物质的量为3.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com