
| A. | 一定存在SO42-、SO32-、NH4+,可能存在Na+ | |
| B. | 一定存在SO42-、SO32-、NH4+,一定不存在Cl-、Na+ | |
| C. | 溶液中可能含有Cl-,且Na+浓度至少为0.15mol•L-1 | |
| D. | c(SO42-)=0.1mol•L-1,c(NH4+)<c(SO42-) |
分析 ①向100mL上述溶液中加入足量BaCl2溶液,反应后将浊液过滤、洗涤、干燥,得沉淀4.50g,若向沉淀中加入过量的盐酸,仍有2.33g沉淀不溶.同时产生能使湿润红色石蕊试纸褪色的气体,可知一定含n(SO42-)=$\frac{2.33g}{233g/mol}$=0.01mol,含n(SO32-)=$\frac{4.50g-2.33g}{217g/mol}$=0.01mol;
②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体0.56L,则一定含n(NH4+)=$\frac{0.56L}{22.4L/mol}$=0.025mol,结合电荷守恒来解答.
解答 解:由上述分析可知,一定含SO42-、SO32-、NH4+,物质的量分别为0.01mol、0.01mol、0.025mol,由电荷守恒可知,0.01mol×2+0.01mol×2>0.025mol×1,则一定含Na+,且Na+浓度至少为$\frac{0.04-0.025}{0.1}$=0.15mol•L-1,不能确定是否含Cl-,c(SO42-)=$\frac{0.01mol}{0.1L}$=0.1mol/L,c(NH4+)=$\frac{0.025mol}{0.1L}$=0.25mol/L,c(NH4+)>c(SO42-),
故选C.
点评 本题考查无机物的推断,为高频考点,把握发生的反应、物质的量的计算、电荷守恒为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的综合应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用CO2合成可降解塑料聚碳酸酯,实现“碳”的循环利用 | |
| B. | 由地沟油加工合成的“生物柴油”与柴油成分相同 | |
| C. | 高温消毒就是用加热的方法使蛋白质变性 | |
| D. | 海水提镁、炼铁、制造玻璃等工业都用到石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
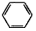
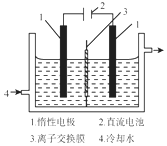 碘被称为“智力元素”科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.
碘被称为“智力元素”科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.| 试验方法 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微电池的负极是Mg | B. | 微电池的负极是Al | ||
| C. | 铝的电极反应式为2H++2e-═H2↑ | D. | 镁的电极反应式为Mg-2e-═Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
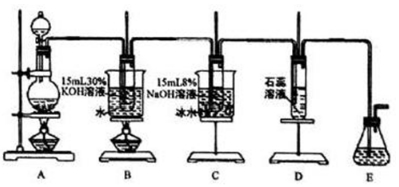
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol•L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 | ------------- |
| 步骤2: 向A试管中加入1-2mL 0.0lmol•L-1 KMnO4溶液,振荡试管 | (1)若溶液褪色,则假设1成立 (2)若溶液不褪色,则假设2或3成立 |
| 步骤3: 向B试管中滴加1-2滴淀粉-KI溶液 | (1)若溶液变蓝,则假设成立 (2)若溶液不变蓝,综合步骤中的(2),则假设2成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .请回答下列问题:
.请回答下列问题:| W | X | Y |
| Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水检验汽油中是否含有不饱和脂肪烃 | |
| B. | 除去苯中混有的苯酚,加入浓溴水,过滤 | |
| C. | 除去乙醇中混有的水,加入金属钠,蒸馏 | |
| D. | 乙烷气体中混有乙烯,通入酸性高锰酸钾溶液,洗气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com