

分析 由流程可知,第一步,KOH和KClO3与MnO2反应,得到K2MnO4,从而可以写出反应方程式为6KOH+3MnO2+KClO3=3K2MnO4+KCl+3H2O,然后加入水溶解分离可溶性物质,得到K2MnO4和KCl;第二步,将滤液酸化,得到高锰酸钾和二氧化锰,为一歧化反应,锰从+6变为+7和+4;反应方程式为3MnO42-+4H+=2MnO4-+MnO2+2H2O,通过过滤分离MnO2和高锰酸钾溶液,最终得到产品,整个过程中MnO2可以循环利用.
(1)操作Ⅱ是固体和液体分离,利用过滤操作分离;
(2)流程中参与反应过程,最后又重新生成的物质可以循环使用;
(3)反应②3MnO42-+4H+=2MnO4-+MnO2+2H2O,依据元素化合价变化分析,氧化产物是元素化合价升高的产物,元素化合价降低的产物为还原产物;
(4)因锰酸根和高锰酸根均具有强氧化性,不能使用盐酸酸化;
(5)由电流流向可知a为正极,铁为活性电极,这里没有参与反应,做阴极故与负极相连,阳极发生氧化反应,锰酸根失电子生成高锰酸根,根据电子得失守恒可以进行相关计算.
解答 解:由流程可知,第一步,KOH和KClO3与MnO2反应,得到K2MnO4,从而可以写出反应方程式为6KOH+3MnO2+KClO3=3K2MnO4+KCl+3H2O,然后加入水溶解分离可溶性物质,得到K2MnO4和KCl;第二步,将滤液酸化,得到高锰酸钾和二氧化锰,为一歧化反应,锰从+6变为+7和+4;反应方程式为3MnO42-+4H+=2MnO4-+MnO2+2H2O,通过过滤分离MnO2和高锰酸钾溶液,最终得到产品,整个过程中MnO2可以循环利用.
(1)操作Ⅱ是固体和液体分离,利用过滤操作分离,所以操作Ⅱ的名称是过滤,故答案为:过滤;
(2)流程中参与反应过程,最后又重新生成的物质可以循环使用,流程中KOH和KClO3与MnO2反应,将滤液酸化,得到高锰酸钾和二氧化锰,整个过程中MnO2可以循环利用,故答案为:MnO2;
(3)反应②为:3MnO42-+4H+=2MnO4-+MnO2+2H2O,反应中锰元素化合价从+6变为+7和+4;得到氧化产物为MnO4-,还原产物为MnO2,物质的量之比为2:1;
故答案为:2:1;
(4)因锰酸根和高锰酸根均具有强氧化性,盐酸中氯离子具有还原性,能被氧化,不能使用盐酸酸化,故答案为:A;
(5)装置图中的电流方向可知,铁为活性电极,这里没有参与反应,做阴极故与负极相连,b做负极,a为正极,石墨电极为阳极发生氧化反应,锰酸根失电子生成高锰酸根,电极反应为:MnO42--e-=MnO4-;根据电子得失守恒可以进行相关计算,若电解过程中收集到2.24L H2 (标准状况),物质的量=$\frac{2.24L}{22.4L/mol}$=0.1mol,电极反应为:2H++2e-=H2↑,结合电子守恒可知:
2MnO4-~2e-~H2,
2 1
0.2mol 0.1mol
得到高锰酸钾质量=0.2mol×158g/mol=31.6g;
故答案为:负;MnO42--e-=MnO4-;31.6.
点评 本题考查了物质制备流程分析判断,电解原理的分析应用,物质性质的理解应用和实验基本操作的掌握,工艺流程题解题的关键是要搞清楚加入什么物质,发生什么反应,如何分离等,通过分析,我们要能够将一个工艺的流程转化为物质的流程,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 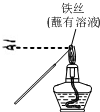 用装置甲检验溶液中是否有K+ | B. |  用装置乙制取并收集少量NH3 | ||
| C. |  用装置丙进行喷泉实验 | D. |  用装置丁加热熔融NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列相关说法中不正确的是( )
,下列相关说法中不正确的是( )| A. | 一定条件下能发生酯化反应 | |
| B. | 一定条件下能发生催化氧化反应 | |
| C. | 不能发生加成反应 | |
| D. | 1mol该物质与Na2CO3溶液反应最多消耗1.5mol Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其氢氧化物中碱性最强的是LiOH | |
| B. | 离子的氧化能力最强的是Cs+ | |
| C. | 原子半径随核电荷数的增大而增大 | |
| D. | 单质的熔点随相对原子质量的增大而增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com