
| A. | 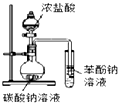 如图证明酸性:盐酸>碳酸>苯酚 | |
| B. | 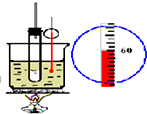 如图实验室制硝基苯 | |
| C. | 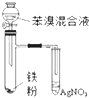 如图验证苯和液溴在催化剂作用下发生取代反应 | |
| D. | 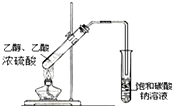 如图实验室制乙酸乙酯 |
分析 A.盐酸具有挥发性,干扰了二氧化碳与苯酚钠的反应;
B.实验室制取硝基苯,用水浴加热;
C.液溴具有挥发性,生成的溴化氢中混有溴,溴能够与硝酸银溶液反应,干扰了溴化氢的检验;
D.乙酸、乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯,可用饱和碳酸钠溶液吸收.
解答 解:A.浓盐酸具有挥发性,挥发出来的氯化氢干扰了二氧化碳与苯酚钠的反应,无法达到实验目的,故A错误;
B.实验室制取硝基苯,用水浴加热,温度不超过60℃,故B正确;
C.液溴乙挥发,溴化氢中含有的溴与水反应生成氢溴酸,可与硝酸银反应生成溴化银沉淀,不能证明是否取代反应,应先通过苯除杂,故C错误;
D.乙酸、乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯,可用饱和碳酸钠溶液吸收,故D正确;
故选AC.
点评 本题考查化学实验方案的评价,为高频考点,题目难度中等,涉及酸性比较、乙酸乙酯、溴苯以及硝基苯的制取等,侧重有机物性质及实验的考查,注意实验操作的评价性分析,有利于实验技能的夯实.


 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=c(H2CO3)+c(HCO3-) | B. | 2c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) | ||
| C. | c(Na+)>c(CO32-)>c(OH-)>c(HCO3-) | D. | c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY2一定是分子晶体 | B. | XY2的电子式可能是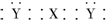 | ||
| C. | XY2水溶液不可能呈碱性 | D. | X可能是ⅣA、ⅤA或ⅥA族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
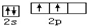 .
. ,该晶体中含微粒间的作用有:离子键和非极性键.
,该晶体中含微粒间的作用有:离子键和非极性键.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 合成氨反应:N2(g)+3H2(g)?2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系增加压强使颜色变深 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 已知反应2NO2(g)?N2O4(g),红棕色气体NO2加压后颜色先变深后变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铁片上:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| C. | 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+═H2O+CO2↑ | |
| D. | 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-═AgCl↓+NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体系压强保持不变 | B. | 混合气体颜色保持不变 | ||
| C. | SO3和NO的体积比保持不变 | D. | 每消耗1molSO3的同时生成1molNO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com