
| A. | 在常温下,向 0.01mol?L-1 的 NH4HSO4 溶液中滴加 NaOH 溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH- )=c(H+) | |
| B. | 25℃时,在 0.1mol?L-1 的 NaHSO4 溶液中,c(H+)=c(OH- )+c(SO42-) | |
| C. | 浓度均为 0.1mol?L-1 的 HF 溶液和 KF 溶液等体积混合:c(F-)+c(HF)=0.2mol/L | |
| D. | 均为 0.1mol?L-1 的 Na2S 溶液和 NaHS 溶液等体积混合:2c(Na+)=3c(HS-)+3c(H2S)+3c(S2-) |
分析 A.当硫酸氢钠与氢氧化钠的物质的量相等时,反应生成硫酸铵和硫酸钠,溶液呈酸性,若为中性,加入的氢氧化钠应该稍过量,则c(Na+)>c(SO42-)>c(NH4+)、c(OH- )=c(H+);
B.根据硫酸氢钠溶液中的电荷守恒和物料守恒分析;
C.根据混合液中的物料守恒判断;
D.根据0.1mol?L-1的Na2S溶液和NaHS溶液中的物料守恒判断.
解答 解:A.常温下,向0.01mol/L NH4HSO4溶液中滴加NaOH溶液至中性,NaOH首先与NH4HSO4电离出的H+作用,因为H+结合OH-的能力比NH4+结合OH-的能量强(原因是产物H2O比NH3•H2O更难电离),当加入等物质的量的NaOH时,正好将H+中和,此时c(Na+)=c(SO42-),但此时溶液中还有NH4+,NH4+水解使溶液呈酸性,因此要使溶液呈中性,则还需继续滴入NaOH,当然到中性时c(OH-)=c(H+),c(Na+)>c(SO42- )>c(NH4+),溶液中离子浓度大小为:c(Na+)>c(SO42-)>c(NH4+)>c(OH- )=c(H+),故A正确;
B.根据硫酸氢钠溶液中的电荷守恒得:c(H+)+c(Na+)=c(OH-)+2c(SO42-),根据物料守恒c(Na+)=c(SO42-)等:c(H+)=c(OH-)+c(SO42-),故B正确;
C.浓度均为0.1mol?L-1 的HF溶液和KF溶液等体积混合,根据物料守恒可得:c(F-)+c(HF)=0.1mol/L,故C错误;
D.浓度均为0.1mol?L-1的Na2S溶液和NaHS溶液等体积混合后,根据物料守恒可得:2c(Na+)=3c(HS-)+3c(H2S)+3c(S2-),故D正确;
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理及其影响为解答关键,注意掌握电荷守恒、物料守恒的含义及其应用方法,试题培养了学生的灵活应用能力.


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 向FeCl2、NaI的混合溶液中加入硫氰化钾溶液,再滴加少量氯水,溶液没有变为红色,说明还原性:Fe2+<I- | |
| B. | 检验AlNH4(SO4)2溶液中的NH4+:取样于试管中,向溶液中加入少量NaOH溶液,加热,用湿润的红色石蕊试纸检验产生的气体 | |
| C. | 检验Na2SO3和Na2SO4的混合溶液中的SO42-:先加足量稀硝酸,再加氯化钡溶液 | |
| D. | 验证碳酸钠溶液显碱性是CO32-导致的:先加酚酞试液,溶液变红,再加硫酸溶液,红色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
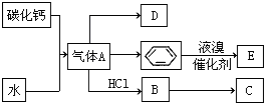 已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空:
已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空: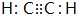 ;C的结构简式
;C的结构简式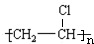 ;
; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr;其反应类型为取代反应.
+HBr;其反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用丁达尔效应可区分溶液和胶体 | |
| B. | 能使湿润的监色石蕊试纸变红的气体是NH3 | |
| C. | 观察钾元素的焰色反应时要透过监色钴玻璃 | |
| D. | 检验溶液中SO42-存在时,先加盐酸酸化,再加氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.336L | B. | 0.224L | C. | 0.168L | D. | 0.504L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上粗硅的制备和提纯 | B. | 工业上从海水中提取溴或镁 | ||
| C. | 工业上采用“侯氏制碱法”制纯碱 | D. | 工业上利用合成氨实现氮的固定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2与足量的铁反应转移的电子数是3NA | |
| B. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| C. | 7.8g Na2O2中含有阴离子数目为0.1NA,与足量水反应时电子转移了0.1NA | |
| D. | 标准状况下33.6L四氯化碳含有的分子数为1.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把CO2通入CaCl2溶液中,有CaCO3沉淀生成 | |
| B. | 把SO2通入Ca(NO3)2溶液中,有CaSO3沉淀生成 | |
| C. | 把CO2通入Ca(ClO)2溶液中,有CaCO3沉淀生成,说明酸性:H2CO3>HClO | |
| D. | 把SO2通入Ca(ClO)2溶液中,有CaSO3沉淀生成,说明酸性:H2SO3>HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com