
分析 1mol水相当于18g水,气体吸热Q=mq=18g×2.26kJ•g-1=40.68KJ;此过程为物态的变化,故△G=0;反应热为1mol水变成蒸气吸收的热量,故△H=Q=40.68KJ;△G=△H-T△S,则△S=$\frac{△H-△G}{T}$=$\frac{40680}{100+273}$KJ/mol=109.06KJ/mol据此进行分析.
解答 解:1mol水相当于18g水,气体吸热Q=mq=18g×2.26kJ•g-1=40.68KJ;此过程为物态的变化,故△G=0;反应热为1mol水变成蒸气吸收的热量,故△H=Q=40.68KJ;△G=△H-T△S,则△S=$\frac{△H-△G}{T}$=$\frac{40680}{100+273}$J/mol=109.06J/mol,
故答案为:40.68KJ;0;40.68KJ;109.06J/mol.
点评 本题考查了求整个过程吸收的热量,吉普斯自由能,反应热,熵,正确使用公式是本题解题的关键,本题难度中等.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 盐卤点豆腐,明矾净水和利用电泳来分离各种氨基酸和蛋白质都与胶体的性质有关 | |
| B. | 人工制造的铝硅酸盐分子筛可用作吸附剂和催化剂载体 | |
| C. | 生物柴油可以用廉价油脂与甲醇发生酯交换反应制得,属于不可再生能源 | |
| D. | 在建的国产航母采用了新的防腐蚀技术,传统的船舶防腐蚀技术是在船体上焊接一些锌块,原理是采用牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
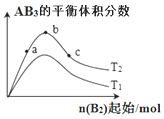 某化学科研小组研究在其它条件不变时,改变某一条件对化学反应:A2(g)+3B2(g)?2AB3(g)的平衡状态的影响时,得到如图所示的变化关系(图中T表示温度,n表示物质的量).下列推论正确的是( )
某化学科研小组研究在其它条件不变时,改变某一条件对化学反应:A2(g)+3B2(g)?2AB3(g)的平衡状态的影响时,得到如图所示的变化关系(图中T表示温度,n表示物质的量).下列推论正确的是( )| A. | 反应速率a>b>c | |
| B. | 若T2>T1,则正反应一定是放热反应 | |
| C. | 达到平衡时,AB3的物质的量大小关系:c>b>a | |
| D. | 达到平衡时,A2转化率的大小关系:a>b>c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解池,阳极Pt,阴极用Cu,纯水做电解液 | |
| B. | 原电池,负极用Cu,正极用石墨,氯化钠溶液做电解液 | |
| C. | 电解池,阳极用Cu,阴极用石墨,H2SO4做电解液 | |
| D. | 电解池,阳极用Cu,阴极用石墨,Na2SO4做电解液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ•mol-1 | |
| B. | 图乙表示一定条件下进行的反应2SO2+O2?2SO3各成分的物质的量变化,t2时刻改变的条件一定是缩小容器体积 | |
| C. | 图丙表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数以ω(B)>ω(A) | |
| D. | 图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁能与酸反应,可用于制作红色涂料 | |
| B. | SO2具有漂白性,可在白葡萄酒中微量添加 | |
| C. | 钠钾合金硬度小,可用作原子反应堆的导热剂 | |
| D. | 酒精能使蛋白质变性,可在医疗上用来杀菌消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com