
| [OH-] |
| [NH3?H2O] |
| [OH-] |
| [NH3?H2O] |
| [OH-] |
| [NH3?H2O] |
| 2×10-11 |
| 0.1 |


科目:高中化学 来源: 题型:
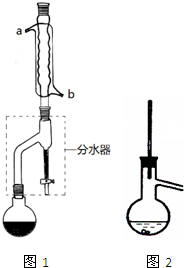 乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为:
乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为:| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/g?mL-1 | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
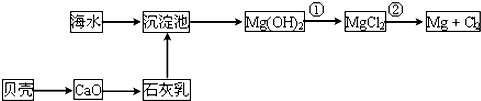
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在0.1 mol?L-1NH3?H2O溶液中:c(NH3H2O)>c(NH4+)=c(OH-)>c(H+) |
| B、0.1 mol?L-1 HCl溶液与0.1 molL-1NaOH溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(Cl-) |
| C、0.1 molL-1NaOH和0.1 mol?L-1NH4Cl溶液等体积混合后:c(Na+)=c(Cl-)>c(H+)>c(OH-) |
| D、25℃时,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸应保存在棕色试剂瓶里 |
| B、铵态氮肥不宜与碱性肥料混合施用 |
| C、常温下铁、铝不与浓硝酸反应 |
| D、NO可用排水法收集,NO2可用向上排空气法收集 |
查看答案和解析>>
科目:高中化学 来源: 题型:
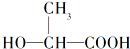 在一定条件下自身可发生缩聚反应,生成一种高聚物
在一定条件下自身可发生缩聚反应,生成一种高聚物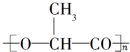 ,用这种新型高聚物制成的餐具,在乳酸菌的作用下,60天内可分解成无害的物质,不会对环境造成污染.在上述聚合反应中,生成的另一种产物是( )
,用这种新型高聚物制成的餐具,在乳酸菌的作用下,60天内可分解成无害的物质,不会对环境造成污染.在上述聚合反应中,生成的另一种产物是( )| A、CO2 |
| B、C2H5OH |
| C、H2O |
| D、CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等.它们的最高价氧化物的水化物依次为甲、乙、丙、丁.下列叙述不正确的是( )
短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等.它们的最高价氧化物的水化物依次为甲、乙、丙、丁.下列叙述不正确的是( )| A、R的氧化物在空气中与其它物质作用可形成光化学烟雾 |
| B、常温下丁的浓溶液可用T单质所制的容器来盛装 |
| C、丁的浓溶液与Q的单质加热发生反应,可生成体积比为1:2的两种气体 |
| D、甲、乙、丙、丁受热均易分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电过程中,Li+从负极区向正极区迁移 |
| B、负极反应式:nLi-ne-?nLi+ |
| C、正极反应式:(CF)n+nLi++ne-?nC+nLiF |
| D、可以用水代替有机溶剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com