
aKMnO4+bKI+fH2SO4——cMnSO4+dI2+eKIO3+gK2SO4+fH2O
试回答下列问题:
①该反应的氧化产物是:________
②若该反应过程中d=e=5,则KMnO4的化学计量数a是_________;转移的电子数为___________。
(2)按下图的装置进行电解实验:A极是铜锌(均匀)合金,B极为纯铜,电解一段时间后,若A极恰好全部溶解,此时B极增加7.

①写出电解时阳极发生的电极方程式:
②A合金中Cu、Zn原子个数比为____________。
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
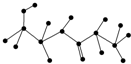 (1)某化合物结构简式如图,请根据所示的化合物回答问题:
(1)某化合物结构简式如图,请根据所示的化合物回答问题:
| 稀硫酸 |
| 稀硫酸 |
| 稀硫酸 |
| 稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com