
| A�� | ���ж�������Ѫ�쵰�ױ����� | B�� | �ⶾʱѪ�쵰�ױ���ԭ | ||
| C�� | ά����CӦ���л�ԭ�� | D�� | �ж�ʱ�������η���������Ӧ |
���� �������ƽ�������ɽ�ѪҺ�еĵ���Ѫ�쵰�������ɸ���Ѫ�쵰�ף����������ξ��������ԣ�FeԪ�صĻ��ϼ����ߣ�ʹ�����ж���ά����C�����������ж�����Ч�ⶾ������ά����C���л�ԭ�ԣ��������ӷ�Ӧ���ɽⶾ���Դ������
��� �⣺A�����ж�������Ѫ�쵰����FeԪ�صĻ��ϼ����ߣ�����������A��ȷ��
B���ⶾʱѪ�쵰����FeԪ�صĻ��ϼ۽��ͣ�����ԭ����B��ȷ��
C��ά����C�ڽⶾ�����У������仹ԭ�ԣ�����ԭ������C��ȷ��
D�����ж�������Ѫ�쵰����FeԪ�صĻ��ϼ����ߣ����������������εĻ��ϼ۽��ͱ���ԭ��������ԭ��Ӧ����D����
��ѡD��
���� ���⿼����������ԭ��Ӧ������������ԭ�����жϣ���ȷ���������ں��ǽⱾ��ؼ�������Ԫ�ػ��ϼ��Ƿ�仯����������ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����β����ڳ����ܽ�ƽ�� | |
| B�� | ��ͨ��������ҺpH����������ʹijЩ�������ӳ��� | |
| C�� | ij��������Һ�г�����ȫ�������������Һ���Ѳ����� | |
| D�� | һ�㣬�ܽ��С����ת�����ܽ�ȸ�С�ģ����ܽ�ȸ�С�IJ���ת�����ܽ��С�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2�� CsCl����CBr4��CF4 | B�� | SiO2�� CsCl CF4 ��CBr4 | ||
| C�� | CsCl����SiO2�� CBr4�� CF4 | D�� | CF4 ��CBr4 CsCl����SiO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͭ��ϡ���ᷴӦ | B�� | ͭ��ϡ���ᷴӦ | ||
| C�� | ľ̿��Ũ���ᷴӦ | D�� | ̼��Ƹ�ϡ���ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£��������������Ƶ�������ʢװŨ�����Ũ���� | |
| B�� | ʵ�����У�ʢװNaOH��Һ���Լ�ƿ����Ƥ�� | |
| C�� | ʵ�����У���������Ͳ���ζ��ܡ�����ƿȷ��ȡһ�������Һ�����ڻ�ѧ��Ӧ�� | |
| D�� | ʵ�����У�ʢ���������ò���ƿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
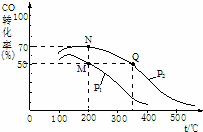 ������Ⱦ������������ȫ���������ŵĿ��⣮��ش��������⣺
������Ⱦ������������ȫ���������ŵĿ��⣮��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
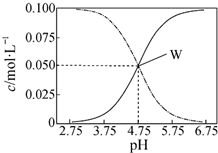
| A�� | pH=5.5��Һ�У�c��CH3COOH����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | W���ʾ��Һ�У�c��Na+���Tc��CH3COO-��+c��CH3COOH�� | |
| C�� | pH=3.5��Һ�У�c��Na+��+c��H+��-c��OH-��+c��CH3COOH��=0.1mol•L-1 | |
| D�� | ��W������ʾ��1.0L��Һ��ͨ��0.05molHCl���壨��Һ����仯�ɺ��ԣ���c��H+���Tc��CH3COOH��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ����HCl����������KMnO4 | |
| B�� | ÿ����1mol Cl2ת�Ƶ��ӵ����ʵ���Ϊ2mol | |
| C�� | �������뻹ԭ�������ʵ���֮��Ϊ1��8 | |
| D�� | ���������뻹ԭ��������ʵ���֮��Ϊ5��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com