
某学生为探究钠与CO2的反应,利用如下装置进行实验。
(已知PdCl2能被CO还原得到黑色的Pd)
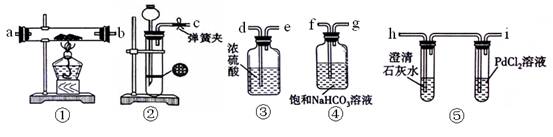
(1)请将上图各装置连接完整
接 , 接 , 接 , 接 。
(2)装置②制备CO2时具有随开随用,随关随停的功能。简述该装置随关随停的理由
;
(3)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是 。
A.NaNO3溶液 B.CCl4 C.苯 D.稀硝酸
(4)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是
,当观察到 现象时才点燃酒精灯。此步操作的目的是 。
(5)反应过程中CO2足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与CO2反应的化学方程式。
① 装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。 。
② 装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,且溶液中还有固体残留。 。
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
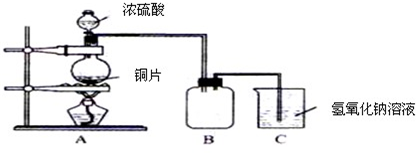
 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生为探究钠与CO2的反应,利用如下装置进行实验。
(已知PdCl2能被CO还原得到黑色的Pd)
(1)请将上图各装置连接完整
接 , 接 , 接 , 接 。
(2)装置②制备CO2时具有随开随用,随关随停的功能。简述该装置随关随停的理由
;
(3)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是 。
A.NaNO3溶液 B.CCl4 C.苯 D.稀硝酸
(4)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是
,当观察到 现象时才点燃酒精灯。此步操作的目的是 。
(5)反应过程中CO2足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与CO2反应的化学方程式。
① 装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。 。
② 装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,且溶液中还有固体残留。 。
查看答案和解析>>
科目:高中化学 来源:2011届湖北省黄冈中学高三最后一次适应性考试(理综)化学部分 题型:实验题
某学生为探究钠与CO2的反应,利用如下装置进行实验。
(已知PdCl2能被CO还原得到黑色的Pd)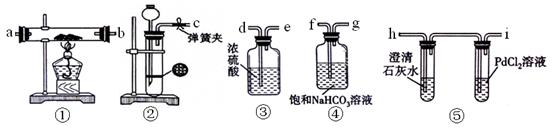
(1)请将上图各装置连接完整
接 , 接 , 接 , 接 。
(2)装置②制备CO2时具有随开随用,随关随停的功能。简述该装置随关随停的理由
;
(3)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是 。
| A.NaNO3溶液 | B.CCl4 | C.苯 | D.稀硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com