
【题目】在一定温度下的定容的容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)![]() C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体总物质的量⑤混合气体的平均相对分子质量⑥混合气体总质量⑦混合气体总体积.
A. ①②③④⑤⑥⑦ B. ①③④⑤ C. ①②③④⑤⑦ D. ①③④⑤⑦
【答案】B
【解析】
当反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆速率之比等于化学化学计量数之比(不同物质),各物质的浓度、质量、体积分数以及百分含量不变,以及由此衍生的一些量也不发生变化,选择判断化学平衡的物理量应随反应进行发生变化,当该物理量不再变化可以说明到达平衡。
①该反应为反应前后气体的物质的量减小的反应,容器体积不变,随反应进行压强降低,当压强不再变化,说明到达平衡,故①正确;
②反应混合物都是气体,总质量不变,容器体积不变,密度自始至终都不变,不能说明到达平衡状态,故②错误;
③随反应进行B的浓度减小,当B的物质的量浓度不再变化,说明到达平衡,故③正确;
④该反应为反应前后气体的物质的量减小的反应,随反应进行混合气体总物质的量减小,混合气体总物质的量不再变化,说明到达平衡,故④正确;
⑤反应混合物都是气体,总质量不变,随反应进行混合气体总物质的量减小,所以随反应进行混合气体的平均相对分子质量增大,当混合气体的平均相对分子质量不再变化,说明到达平衡,故⑤正确;
⑥反应混合物都是气体,混合气体总质量不发生变化,不能说明到达平衡,故⑥错误;
⑦容器的体积不变,混合气体总体积不变,不能说明到达平衡,故⑦错误;
①③④⑤正确,故选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知SO3分解反应为2SO3(g)2SO2(g)+O2(g)。在1.0L密闭容器中加入10mol SO3(g),在一定温度进行上述反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/kPa | 400 | 412 | 422 | 440 | 469 | 518 | 538 | 560 | 560 |
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为_____(填字母)。
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为_____,该温度下的平衡常数Kw=_____
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPamin﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=_____kPa,v(SO3)=_____kPamin﹣1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右图所示,电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
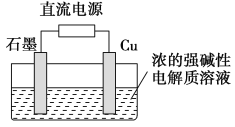
A. 铜电极发生还原反应 B. 石墨电极上产生氢气
C. 铜电极接直流电源的负极 D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 实验室中常用排饱和食盐水的方法收集Cl2
B. 对CO(g)+NO2(g)![]() CO2(g)+NO(g),平衡体系增大压强可使颜色变深
CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C. 升高温度能够促进水的电离
D. 在含有Fe(SCN)3的红色溶液中加少量铁粉,振荡静置,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三种溶液,进行如下操作:
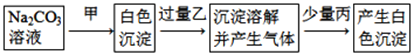
则甲、乙、丙三种溶液中加的溶质可能是( )
A.BaCl2、H2SO4、KClB.CaCl2、HNO3、AgNO3
C.CaCl2、HNO3、NaClD.BaCl2、HCl、Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷(C10H16)的结构如图1所示,它可以看成四个等同的六元环组成的空间构型。立方烷(C8H8)的结构如图2所示。其中金刚烷的二氯代物和立方烷的六氯代物的同分异构体分别是 ( )

A. 4种和1种 B. 5种和3种
C. 6种和3种 D. 6种和4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。现有Ca(OH)2溶液,向其溶液中逐渐通入CO2。则下列四个图中,能比较准确地反映出溶液的导电能力和通入CO2气体量的关系的是(x轴表示CO2通入的量,y轴表示导电能力)
A. 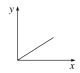 B.
B. 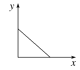
C. 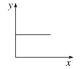 D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.Fe(OH)3胶体可使水中悬浮物凝聚沉淀,是城市饮用水处理新技术。
(1)实验室如何制取Fe(OH)3胶体,请简述操作___,相应的化学方程式是____。
(2)向Fe(OH)3胶体中逐滴加入硅酸胶体,逐渐出现红褐色沉淀,出现该现象的原因是____。
(3)除去胶体中混有的FeCl3和HCl的方法是___,如何验证胶体已净化完全,请简述方法___。
Ⅱ.已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为____mol·L-1(保留小数点后一位)。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下面操作造成所配溶液浓度偏高的是___(填序号)。
A.容量瓶用蒸馏水洗涤后未进行干燥处理,底部有少量水残留
B.向容量瓶加水定容时眼睛俯视液面
C.烧杯溶解固体后,用蒸馏水润洗2-3次,将部分洗涤液转入容量瓶中
D.定容摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 已知常温下部分弱电解质的电离平衡常数如下表:
化学式 | HF | HClO | H2CO3 | NH3·H2O |
电离常数 | 6.8×104 | 4.7×108 | K1=4.3×107 K2=5.6×1011 | Kb=1.7×105 |
(1)常温下,PH相同的三种溶液①NaF溶液 ②NaClO溶液 ③Na2CO3溶液,其物质的量溶度由大到小的顺序是___________(填序号)
(2)25°C时,PH=4的NH4Cl溶液中各离子浓度的大小关系为___________________
(3)0.1 mol/L的NaClO溶液和0.1 mol/L的NaHCO3溶液中,c(ClO-)________ c(HCO3-)(填“>,<,=”)可使上述两种溶液PH相等的方法是___________(填代号)
a.向NaClO溶液中加适量的水 b.向NaClO溶液中加适量的NaOH
c.向NaHCO3溶液中加适量的水 d. 向NaHCO3溶液中加适量的NaOH
(4)向NaClO溶液中通入少量的CO2,所发生的离子方程式为_________
(5)常温下,0.1mol/L的氨水和0.1mol/L的NH4Cl溶液等体积混合,判断混合溶液的酸碱性____________(填“酸性”“碱性”“中性”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com