
| A、在25℃时,若溶液呈中性,则pH=7,AG=1 |
| B、在25℃时,若溶液呈酸性,则pH<7 AG<0 |
| C、在25℃时,若溶液呈碱性,则pH>7 AG>0 |
| D、在25℃时,溶液的pH与AG的换算公式为AG=2(7-pH) |
| C(H+) |
| C(OH-) |
| KW |
| C(H+) |
| C(H+) |
| C(OH-) |
| ||
| C(H+) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是物质的数量单位 |
| B、58.5gNaCl溶解在1L水中,得到溶液的物质的量浓度为1mol/L |
| C、标况下,1molCCl4所占的体积约为22.4L |
| D、12g12C含有的碳原子数约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 molH2的质量是1 g |
| B、1 mol HCl的质量是36.5 g?mol-1 |
| C、Cl2的摩尔质量等于它的相对分子质量 |
| D、硫酸根离子的摩尔质量是96 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解质本身不一定能导电 |
| B、在溶液中,导电能力弱的电解质不一定是弱电解质 |
| C、纯净的强电解质在液态时,有的导电,有的不导电 |
| D、SO2的水溶液能导电,所以SO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 表示碳原子,用
表示碳原子,用 表示氧原子,用
表示氧原子,用 表示氮原子,如图为气体转换的微观过程.请你根据图示回答下列问题:
表示氮原子,如图为气体转换的微观过程.请你根据图示回答下列问题: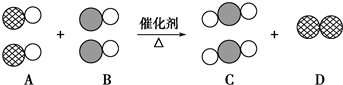
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用广泛pH试纸测得氯水的pH为2 |
| B、用托盘天平称取10.50g干燥的NaCl固体 |
| C、配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏高 |
| D、制备Fe(OH)2时,向FeSO4溶液中滴入NaOH溶液时,胶头滴管不能伸入液面以下 |
查看答案和解析>>
科目:高中化学 来源: 题型:
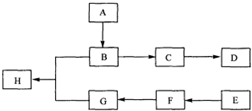
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com