

| A. | 乙醇和浓硫酸,共热到170℃时断键②⑤ | |
| B. | 乙醇和浓硫酸,共热到140℃时断键①④ | |
| C. | 乙醇和金属钠的反应断键① | |
| D. | 乙醇在Cu催化下与O2反应时断键①③ |
分析 A.乙醇和浓硫酸,共热到170℃发生消去反应生成乙烯;
B.乙醇和浓硫酸,共热到140℃时发生取代反应生成乙醚;
C.乙醇和金属钠反应生成乙醇钠和氢气;
D.乙醇在Cu催化下与O2反应生成乙醛.
解答 解:A.乙醇和浓硫酸,共热到170℃发生消去反应生成乙烯,-OH转化为碳碳双键,断键②⑤,故A正确;
B.乙醇和浓硫酸,共热到140℃时发生取代反应生成乙醚,断裂的化学键为①或②,故B错误;
C.乙醇和金属钠反应生成乙醇钠和氢气,O-H断裂,则断键①,故C正确;
D.乙醇在Cu催化下与O2反应生成乙醛,-OH转化为-CHO,断键①③,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意反应中官能团的变化及化学键的断裂,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
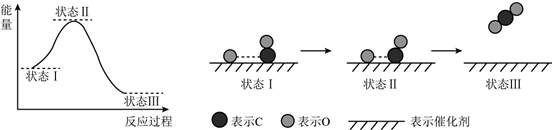
| A. | CO和O生成CO2是吸热反应 | |
| B. | 在该过程中,CO断键形成C和O | |
| C. | 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 | |
| D. | CO和O生成了具有极性共价键的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度计要插入反应混合液中 | |
| B. | 圆底烧瓶中要放入少量碎瓷片 | |
| C. | 圆底烧瓶中注入酒精和稀硫酸的体积为1:3 | |
| D. | 加热时使液体温度迅速升高到170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Cl-、S2- | B. | Cl-、CO、Na+ | C. | Fe3+、SO42-、NO3- | D. | Fe2+、O2、H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
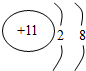 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

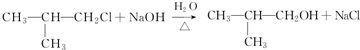 ,反应类型为水解(取代)反应.
,反应类型为水解(取代)反应. ,反应类型为酯化(取代)反应.
,反应类型为酯化(取代)反应.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com