
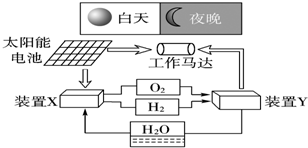
| A. | 二氧化硅是太阳能电池的光电转换材料 | |
| B. | 装置X能实现燃料电池的氢气和氧气再生 | |
| C. | 装置Y中负极的电极反应式为:O2+2H2O+4e-═4OH- | |
| D. | 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
分析 A.硅电池是太阳能电池的光电转换材料;
B.X装置是电解池,电解水生成氢气和氧气;
C.负极上氢气失电子发生氧化反应;
D.化学能与电能间不可能完全转化,还有部分转化为其它能.
解答 解:A.硅元素处于金属和非金属元素分界线处,具有金属性和非金属性,可以作硅太阳能电池,所以硅电池是太阳能电池的光电转换材料,二氧化硅作光导纤维材料,故A错误;
B.X装置是电解池,电解水生成氢气和氧气,所以装置X能实现燃料电池的氢气和氧气再生,故B正确;
C.负极上氢气失电子发生氧化反应,正极上氧气得电子发生还原反应,Y中正极的电极反应式为:O2+2H2O+4e-═4OH-,故C错误;
D.化学能与电能间不可能完全转化,还有部分转化为其它能,所以装置X、Y形成的子系统能实现物质的零排放,但不能实现化学能与电能间的完全转化,故D错误;
故选B.
点评 本题考查化学电源新型电池,侧重考查原电池原理及能量转化,明确图中发生的反应及能量转化方式,注意电极反应式的书写要结合电解质溶液酸碱性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O族 |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A | ||||||
 ,
, G元素的最高价氧化物电子式
G元素的最高价氧化物电子式
 ;H的氢化物的电子式
;H的氢化物的电子式
| 元素 | 实验设计 | 现象 | 结论 |
| B | 分别在两个盛有滴加酚酞的水的烧杯中加入形状相同的Na和K,观察现象 | K在反应中伴随轻微爆炸,钾比钠的反应更剧烈 | 金属性: K>Na |
| F |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 欧洲和北美洲的一些大城市上空二氧化氮浓度很高,其原因是这些地区硝酸工业发达 | |
| B. | 大气污染物中的二氧化硫能引起呼吸道疾病 | |
| C. | 天然的药物无任何毒副作用,可长期服用 | |
| D. | 长期食用二氧化硫含量超标的食品会破坏维生素B1,可通过服入碱性物质(如NaOH)的方法来消除二氧化硫中毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向烧碱溶液中加入铝:Al+2OH-=AlO2-+H2↑ | |
| B. | 用过量氨水吸收烟道气中的SO2:SO2+2NH3•H2O=SO32-+2NH4++H2O | |
| C. | 将饱和FeCl3溶液滴入废水中制取Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3↓+3H+ | |
| D. | 用Fe2+将饮用水中少量ClO2-还原成为Cl-:4Fe2++ClO2-+4H+=4Fe3++Cl-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
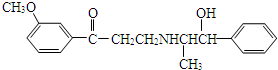
| A. | 该分子中含有酚羟基 | |
| B. | 该物质可以和浓氢溴酸发生取代反应 | |
| C. | 该物质可以和银氨溶液发生银镜反应 | |
| D. | 该分子苯环上的一氯取代物有6种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com