
【题目】某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应).请回答下列问题:

(1)A、B中的反应物分别是浓盐酸和MnO2.写出所发生的化学方程式_____,进入装置C的气体中所含杂质是_____、_____.
(2)漂白粉的有效成分是_____(填化学式);D中所发生的化学反应的离子方程式是______.
(3)此实验所得漂白粉的Ca(ClO)2产率偏低.该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_____
②为避免另一副反应的发生,应采取的措施是_____.
(4)若将该实验中残留的Cl2,缓慢通入KI溶液至过量,则溶液先变黄后变无色,且可检测到HIO3;写出并配平该“变无色”反应的化学方程式:5Cl2+I2+_____→_____若将KI改为KBr溶液,则溶液变为_____色,未检测到HBrO3的存在.由上述事实推测,Cl2、HIO3、HBrO3的氧化性由强到弱的次序是_____.
【答案】MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O; HCl H2O Ca(ClO)2 Cl2+2OH﹣=Cl﹣+ClO﹣+H2O 将U型管置于冷水浴中 可以在B、C之间连接一个盛有饱和食盐水的洗气瓶; 6H2O 2HIO3+10HCl 橙黄 HBrO3>Cl2>HIO3
MnCl2+Cl2↑+2H2O; HCl H2O Ca(ClO)2 Cl2+2OH﹣=Cl﹣+ClO﹣+H2O 将U型管置于冷水浴中 可以在B、C之间连接一个盛有饱和食盐水的洗气瓶; 6H2O 2HIO3+10HCl 橙黄 HBrO3>Cl2>HIO3
【解析】
(1)浓盐酸与二氧化锰在加热条件下生成二氯化锰和氯气;浓盐酸易挥发,制得的氯气中混有氯化氢气体和水蒸气;
(2)漂白粉的有效成分为次氯酸钙;氯气有毒,用氢氧化钠吸收,生成氯化钠和次氯酸钠;
(3)因为温度高时易生成Ca(ClO3)2,所以避免此反应发生。可以采取降温措施,盐酸易挥发,氯化氢与氢氧化钙反应;
(4)由题目信息可知,Cl2将溶液中的I2氧化成HIO3,自身被还原为HCl,配平书写方程式;氧化剂和还原剂反应生成氧化产物和还原产物,氧化剂氧化性大于氧化产物的氧化性。
解:(1)A、B中的反应物分别是浓盐酸和MnO2.发生的化学方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;浓盐酸易挥发,制得的氯气中混有氯化氢气体和水蒸气;
MnCl2+Cl2↑+2H2O;浓盐酸易挥发,制得的氯气中混有氯化氢气体和水蒸气;
故答案为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;HCl;H2O;
MnCl2+Cl2↑+2H2O;HCl;H2O;
(2)漂白粉的有效成分为次氯酸钙Ca(ClO))2;D中为氢氧化钠,吸收氯气,发生的离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;
故答案为:Ca(ClO)2;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;
(3)①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免副反应发生,应该降低温度,所以可以采取将U型管置于冷水浴中的措施;
故答案为:将U型管置于冷水浴中;
②盐酸易挥发,加热过程中生成的氯气中含有氯化氢,氯化氢能和碱反应,所以反应方程式为:Ca(OH))2+2HCl=CaCl2+2H2O,为避免副反应发生,可以在B、C之间连接一个盛有饱和食盐水的洗气瓶;
故答案为:在B、C之间连接一个盛有饱和食盐水的洗气瓶;
(4)由题目信息可知,Cl2将溶液中的I2氧化成HIO3,自身被还原为HCl,反应方程式为:5Cl2+I2+6H2O=2HIO3+10HCl,碘被氧化生成生成HIO3,说明氧化性Cl2>HIO3,KI溶液换成KBr溶液,滴加氯水,溶液呈橙黄色;滴加氯水至过量,颜色没有变化,可说明氯气不未检测到HBrO3的存在,能将溴进一步氧化,说明氧化性HBrO3>Cl2,则有HBrO3>Cl2>HIO3;
故答案为:6H2O;2HIO3+10HCl;橙黄;HBrO3>Cl2>HIO3.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下面关于原电池的说法,正确的是
A.在正极上发生氧化反应 B.化学性质较活泼的一极为负极
C.在外电路中电子流出的极为正极 D.原电池是将电能转化为化学能的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经多年勘测,2018年11月23日省自然资源厅发布消息称在皖江地区发现特大铜矿床,具有重大实际意义。以黄铜矿(主要成分为CuFeS2,含有少量PbS、Al2O3、SiO2)为原料制取胆矾的流程如图:
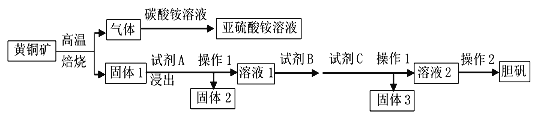
已知:常温下Ksp[Fe(OH)3]=8.0×10-38, Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为______,硫元素在周期表中的位置是______________。
写出上述流程中生成亚硫酸铵的离子方程式:____________。
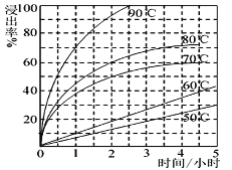
(2)最适合的试剂A是________(写化学式)溶液,固体2的成份为PbSO4和_______。当试剂A的浓度为6mol·L-1时 ,“浸出”实验中,铜的浸出率结果如图所示。所采用的最佳实验条件(温度、时间)为_______________。
(3)最适合的试剂B是_______(填序号),最适合的试剂C是______(填序号),固体3的成份为_________________________。
a.Cl2 b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2 溶液 f.K2CO3
(4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和_______,操作2的步骤为_______________,_______________,过滤、洗涤。
(5)根据已知图像信息,请计算:当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为______。
(提示:当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去氯化钠样品中的杂质碳酸钠,某兴趣小组最初设计了如下所示方案进行实验:

关于该实验的说法错误的是( )
A.用过滤的方法分离出沉淀A,沉淀A为CaCO3
B.固体B 为纯净的NaCl
C.蒸发时用玻璃棒搅拌,防止飞溅
D.在混合物溶液中加过量盐酸能实现该实验的目的,且更简便
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
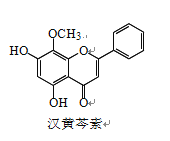
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。

实验步骤如下:
①连接好实验装置,检查装置的气密性。
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279. 7 mL。
⑤准确称量试管和残留物的质量为15. 55 g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?____________________________________________。
(2)以下是测量收集的气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同;
②使试管和广口瓶内气体都冷却至室温;
③读取量筒内液体的体积。
这三步操作的正确顺序是_________________(请填写步骤代号)。
进行③的实验操作时,若仰视读数,则读取氧气的体积_______(填“偏大”“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是_____mol;实验测得氧气的气体摩尔体积是______(保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.1000 mol/L NaOH溶液滴定未知浓度的盐酸溶液,操作可分解为如下几步:
A.用蒸馏水洗干净滴定管;B. 用待测定的溶液润洗酸式滴定管;C.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞;D.另取锥形瓶,再重复操作一次;E.检查滴定管是否漏水;F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。完成以下填空:
(1)正确操作的顺序是(用序号字母填写)_____________。
(2)操作F中应该选择图中________滴定管(填标号)。
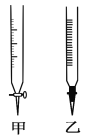
(3)滴定时边滴边摇动锥形瓶,眼睛应观察________。
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是____________________________。
(4)滴定结果如表所示:
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 20 | 1.02 | 21.03 |
2 | 20 | 2.00 | 25.00 |
3 | 20 | 0.60 | 20.60 |
滴定中误差较大的是第________次实验,造成这种误差的可能原因是________。
A. 碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B. 滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C. 滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D. 达到滴定终点时,仰视溶液凹液面最低点读数
E. 滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为________mol/L。
(6)如果准确移取20.00 mL 0.1000 mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用Na2O2作为供氧剂:
(1)实验室常用加热钠的方法制备Na2O2,Na2O2是_______色固体,实验室制备Na2O2的化学方程式_______,试写出Na2O2与CO2反应的化学方程式________。
(2)现有mg含有Na2O杂质的Na2O2试样。(可供选用的反应物只有CaCO3固体,6molL﹣1 盐酸和蒸馏水)请从如图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度。

请填写下列空白:
①写出实验中Na2O2和Na2O分别发生反应的化学方程式__________、__________。
②应选用的装置的连接顺序应是___________。
③若开始时测得样品的质量为2.0g,反应结束后测得生成气体的体积为224mL(标准状况),计算出试样中Na2O2的纯度为:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com