
��14�֣���Դ��ȱ���������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϡ���ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯ͼ��
CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯ͼ��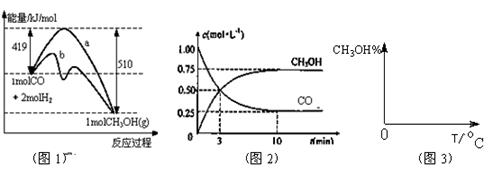
��ش��������⣺
��1���ڡ�ͼ1���У����� ���a����b������ʾʹ���˴������÷�Ӧ���� ������ȡ����ȡ�����Ӧ��
��2�����ݡ�ͼ2���жϣ�����˵������ȷ����
| A����ʼ�����COΪ1mol |
| B������COŨ�ȣ�CO��ת�������� |
| C��������ѹǿ�㶨ʱ����Ӧ�Ѵ�ƽ��״̬ |
| D�������¶Ⱥ��ܱ������ݻ����䣬�ٳ���1molCO��2molH2���ٴδﵽƽ��ʱn(CH3OH)/n(CO)������ |
 CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ �������������������䣬����Ӧ��ϵ���£���÷�Ӧ�Ļ�ѧƽ�ⳣ���� �����������С�����䡱����
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ �������������������䣬����Ӧ��ϵ���£���÷�Ӧ�Ļ�ѧƽ�ⳣ���� �����������С�����䡱����
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com