
分析 (1)酸性环境下双氧水具有氧化性,能将金属铜氧化,铜离子催化双氧水分解;
(2)物质的氧化性与溶液的酸碱性有关.
解答 解:(1)酸性环境下双氧水具有氧化性,能将金属铜氧化,其反应的方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O,反应生成的铜离子能够催化双氧水分解,其反应的方程式为:2H2O2$\frac{\underline{\;Cu_{2}+\;}}{\;}$2H2O+O2↑;
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;2H2O2$\frac{\underline{\;Cu_{2}+\;}}{\;}$2H2O+O2↑;
(2)物质的氧化性与溶液的酸碱性有关,R3++Cl2+6OH-=RO3-+2Cl-+3H2O 是在碱性条件下发生的,5RO3-+2Mn2++14H+=5R3++2MnO4-+7H2O是在酸性条件下发生的,反应条件不同,不能比较物质的氧化性强弱;
故答案为:不能;两个反应是不在相同条件下进行的.
点评 本题考查了氧化还原反应、方程式的书写、氧化性的比较,题目难度不大,注意把握氧化性比较时反应条件要相同.


科目:高中化学 来源: 题型:选择题
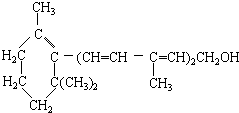
| A. | 维生素A分子含有氢原子数为奇数 | |
| B. | 维生素A的分子中含有苯环结构 | |
| C. | 1mol维生素A在催化剂作用下,可以和5molH2完全加成 | |
| D. | 维生素A属于醇,是一种水溶性维生素,可以发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH大小顺序①>④>③>② | |
| B. | C(NH3•H2O)大小顺序:②>④>③>① | |
| C. | 混合溶液④中存在C(NH3•H2O)+C(CO32-)+C(H+)=C(OH-)+C(H2CO3) | |
| D. | 混合溶液③中水的电离被促进,其中C(H+)和C(OH-)均大于1.0×10-7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的化学活泼性:W<X<Y<Z | B. | 单质的氧化能力:W>X>Y>Z | ||
| C. | 原子最外层电子数:W<X<Y<Z | D. | 元素的最高化合价:W<X<Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
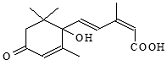
| A. | 分子式C15H21O4 | |
| B. | 既能发生加聚反应,又能发生缩聚反应 | |
| C. | 分子中有三种官能团 | |
| D. | 既能使氯化铁溶液发生显色反应,又能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+ | |
| B. | 由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+3OHˉ=Al(OH)3 | |
| C. | 由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Fe-2e-=Fe2+ | |
| D. | 由Fe、Cu、浓硝酸组成的原电池,开始时其负极反应式为:Cu-2e-=Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 | |
| B. | 浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 | |
| C. | 硝酸与金属反应时,主要是+5价的氮元素得电子 | |
| D. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ②③ | C. | ①④ | D. | ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com