
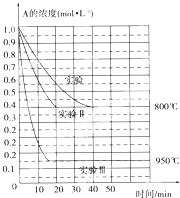
 在一个体积为1L的密闭容器中发生某化学反应:2A(g)?B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在950℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示.试回答下列问题:
在一个体积为1L的密闭容器中发生某化学反应:2A(g)?B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在950℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示.试回答下列问题:| △c |
| △t |
| 0.15 |
| 20 |
| 1-0.4 |
| 1 |


科目:高中化学 来源: 题型:
| A、某可溶性物质的摩尔质量大于18g/mol,则该物质的浓溶液的密度一定大于1g/cm3 | ||
| B、某温度时,氯化钠饱和溶液的质量分数为a%,该温度下氯化钠的溶解度为Sg,则a一定大于S | ||
| C、将90%的H2SO4与10%的H2SO4溶液等体积混合,所得混合溶液中H2SO4的质量分数大于50% | ||
D、饱和KCl溶液密度为ρg/cm3,物质的量浓度为c mol/L,则此溶液中KCl的质量分数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钠在水中的电离方程式:NaHCO3═Na++H++CO32- |
| B、金属Na投入水中:2Na+2H2O═2Na++2OH-+H2↑ |
| C、硫酸与氢氧化钡溶液反应:H++OH-=H2O |
| D、实验室用氢氧化钠溶液吸收多余的Cl2:Cl2+OH-=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol、64mol、24mol |
| B、64mol、2mol、24mol |
| C、32mol、50mol、12mol |
| D、16mol、50mol、24mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com