
分析 (1)碘的提取和含碘量测定应先:C.取干燥的紫菜m g于坩埚中灼烧,A.将灼烧后的紫菜灰溶于水,配成悬浊液,过滤;D.向滤液中滴加硫酸酸化的3%的H2O2溶液a mL,充分反应;B.将水溶液和试剂甲加入分液漏斗中,震荡后静置,放出下层溶液备用;E.对下层溶液进行某操作,得到碘单质并回收试剂甲;
(2)步骤D中发生的是过氧化氢氧化碘离子为碘单质;实验过程中碘离子、过氧化氢都可以和高锰酸钾溶液发生反应使之褪色;
(3)对下层溶液进行某操作,得到碘单质并回收试剂甲,利用物质的沸点不同通过蒸馏方法得到;
(4)所加H2O2溶液恰好完全反应完全,依据化学方程式定量关系计算碘离子物质的量计算碘元素质量分数.
解答 解:(1)碘的提取和含碘量测定应先:C.取干燥的紫菜m g于坩埚中灼烧,A.将灼烧后的紫菜灰溶于水,配成悬浊液,过滤;D.向滤液中滴加硫酸酸化的3%的H2O2溶液a mL,充分反应;B.将水溶液和试剂甲加入分液漏斗中,震荡后静置,放出下层溶液备用;E.对下层溶液进行某操作,得到碘单质并回收试剂甲,实验步骤进行合理的排序为:CADBE;
故答案为:CADBE;
(2)步骤D中发生的是过氧化氢氧化碘离子为碘单质,反应的离子方程式为:2H++H2O2+2I-=I2+2H2O;实验过程中碘离子、过氧化氢都可以和高锰酸钾溶液发生反应使之褪色;步骤D中的H2O2可能有剩余,取少量酸性高锰酸钾溶液,向其中滴加D中反应后的溶液,若溶液褪色则说明还剩余H2O2.小组乙同学认为该结论存在不严谨的地方,请指出你认为不严谨的地方,若步骤D中I-未反应完,剩余的I-也可使高锰酸钾溶液褪色;
故答案为;2H++H2O2+2I-=I2+2H2O;若步骤D中I-未反应完,剩余的I-也可使高锰酸钾溶液褪色;
(3)对下层溶液进行某操作,得到碘单质并回收试剂甲,利用物质的沸点不同通过蒸馏方法得到;
故答案为:蒸馏;
(4)所加H2O2溶液恰好完全反应完全,依据化学方程式定量关系计算碘离子物质的量计算碘元素质量分数;
2H++H2O2+2I-=I2+2H2O
1 2
aml×1g/cm3×3% n
n=$\frac{aml×1g/c{m}^{3}×3%}{34g/mol}×2$;
则该紫菜中碘的含量可表示=$\frac{\frac{a×3%}{34}mol×2×127g/mol}{\frac{m}{100}g}$=$\frac{\frac{a×3%}{34}×2×127}{\frac{m}{100}}$;
故答案为:$\frac{\frac{a×3%}{34}×2×127}{\frac{m}{100}}$.
点评 本题考查物质含量的测定,为高考常见题型,题目涉及对实验原理与操作步骤的理解、化学计算、物质组成的测定等,难度较大,是对所需知识的综合运用,需要学生具有扎实的基础知识与分析问题、解决问题的能力,理解实验原理是解答的关键.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | 钠原子与氯原子反应生成NaCl后,其结构的稳定性增强 | |
| B. | 阴、阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距离相当小 | |
| C. | 失电子难的原子获得电子的能力一定强 | |
| D. | 任何离子键在形成的过程中必定有电子的得与失 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 硝基胍是硝化纤维火药、硝化甘油火药的掺合剂、固体火箭推进剂的重要组分,其结构如图所示(“→”是一种特殊的共价单键).下列有关硝基胍的说法正确的是( )
硝基胍是硝化纤维火药、硝化甘油火药的掺合剂、固体火箭推进剂的重要组分,其结构如图所示(“→”是一种特殊的共价单键).下列有关硝基胍的说法正确的是( )| A. | 硝基胍分子中只含极性键,不含非极性键 | |
| B. | 硝基胍中有C、H、O、N四种元素,属于氨基酸 | |
| C. | 硝基胍分子中σ键与π键的个数比是5:1 | |
| D. | 10.4 g该物质含有1.1×6.02×1023个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若它们均为金属元素,则X、Y与氧元素组成的物质一定是碱性氧化物 | |
| B. | 若它们的原子最外层电子数之和为11,则它们均为非金属元素 | |
| C. | 若它们均不是金属元素,则非金属性:Z>Y>X | |
| D. | Z元素的最高化合价不一定高于X元素的最高化合价 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
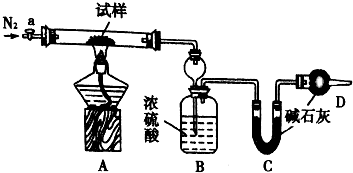 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
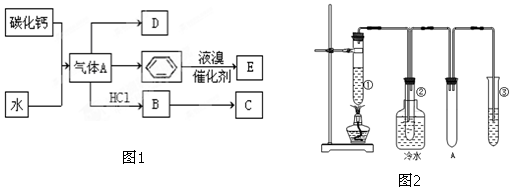
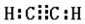 ;
;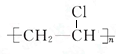 ,其反应类型为加聚反应.
,其反应类型为加聚反应.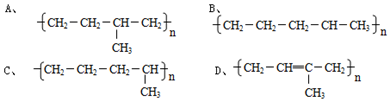
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
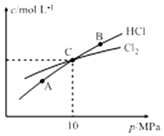 氯氨是氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2C1、NHC12和NC13),副产物少于其它水消毒剂.
氯氨是氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2C1、NHC12和NC13),副产物少于其它水消毒剂. .
.| 化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
| 键能(kJ/mol) | 391.3 | 243.0 | 191.2 | 431.8 |
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(Cl2)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(Cl2)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com