
化学在生产和生活中有着重要的作用。下列有关说法不正确的是
A.铝需经过特别处理才具有抗腐蚀能力
B.“地沟油”经过加工处理可用来制肥皂
C.嫦娥系列卫星中使用的碳纤维,是一种新型
D.只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂
科目:高中化学 来源:2014-2015浙江省台州市高一下学期第一次月考化学试卷(解析版) 题型:实验题
(8分)有人设计了如图所示实验,以确认某混合气体中含有C2H4和SO2。
混合气体
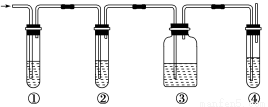
所需试剂有
A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.酸性高锰酸钾溶液
试回答下列问题:
(1)写出图中①、②、③、④装置可盛放的试剂(将上述有关试剂的序号填入空格内):
①________,②________,③________,④________。
(2)使用装置②的目的是_____________________________________________________。
(3)确定乙烯存在的现象是____________________________________________________
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是
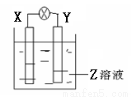
X | Y | Z | |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸 |
C | 锌 | 铜 | 硝酸银溶液 |
D | 碳 | 锌 | 硝酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列离子中,所带电荷数与该离子的核外电子层数相等的是
A.Al3+ B.Mg2+ C.Be2+ D.H+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北武汉市高三毕业生四月调研测试理综化学试卷(解析版) 题型:选择题
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是
A.原子半径的大小顺序:rY> rX >rQ>rW
B.X、Y的最高价氧化物的水化物之间不能发生反应
C.Z元素的氢化物稳定性大于W元素的氢化物稳定性
D.元素Q和Z能形成QZ2型的共价化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省八市高三教学质量监测考试理科综合化学试卷(解析版) 题型:简答题
(15分)铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集了的气体体积均小于2.24 L(标准状况),最主要的原因是__________,所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因______________。
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox 和用于除去废气的转化关系如图
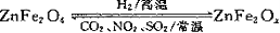 。
。
若上述转化反应巾消耗的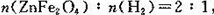 ,x的值为____________________。请写出 ZnFe2Ox与NO2 反应的化学方程式________________________(x用前一问求出的具体值)。
,x的值为____________________。请写出 ZnFe2Ox与NO2 反应的化学方程式________________________(x用前一问求出的具体值)。
(3)LiFePO4(难溶干水)材料被视为最有前途的锂离子电池材料之一。
①以FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,,该反应还生成一种可燃性气体,则反应方程式为____________________________.
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负桩隔开)工作原理为 。则放电时正极上的电极反应式为____________________.
。则放电时正极上的电极反应式为____________________.
(4)已知25℃时,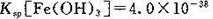 ,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加人________ml,2 mol/L。的盐酸(忽略加入盐酸体积)。
,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加人________ml,2 mol/L。的盐酸(忽略加入盐酸体积)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省八市高三教学质量监测考试理科综合化学试卷(解析版) 题型:选择题
分子式为C5H8O2 的有机物,能使溴的CCl4 溶液褪色,也能与NaHCO3 溶液反应生成气体,则符合上述条件的同分异构体(不考虑立体异构)最多有
A.8种 B.7种 C.6种 D.5种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:填空题
(16分)由有机物Ⅰ合成Ⅳ(香豆素)的合成路线如下:
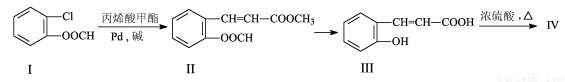
回答下列问题:
(1)写出分子式:丙烯酸甲酯____________________;
(2)写出反应类型:Ⅰ→Ⅱ ;若要Ⅱ→Ⅲ的反应完全,则Ⅱ→Ⅲ 反应需要的条件是 ;
(3)已知化合物Ⅳ的相对分子质量为146,写出结构简式:Ⅳ ;
(4)化合物V是Ⅲ的一种同分异构体,V有如下特征:分子中除苯环外,无其它环状结构;在核磁共振氢谱图中,有四个吸收峰;能发生银镜反应;1 mol V最多能与2mol的NaOH反应。V的结构简式为________________;
(5)根据已有知识并模仿香豆素合成路线的相关反应,试写出以氯苯和丙烯(CH2=CH-CH3)为原料,合成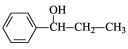 的化学方程式 (无机试剂任选)。
的化学方程式 (无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市高三3月月考化学试卷(解析版) 题型:实验题
(本题14分)(Ⅰ)二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
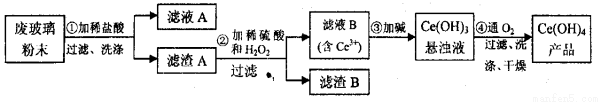
(1)洗涤的目的主要是为了除去Cl-和___________(填离子符号),检验该滤渣A洗净的方法是_____________________。
(2)第②步反应的离子方程式是____________________________。
(3)取上述流程中得到的Ce(OH)4产品0.536 g,加硫酸溶解后,用0.1000mol·L-1FeSO4标准溶液滴定终点时(铈被还原为Ce3+),消耗25.00mL标准溶液,该产品中Ce(OH)4的质量分数为_____________。
(Ⅱ)氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
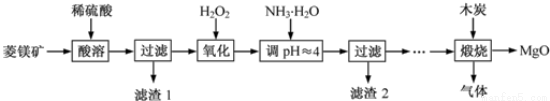
(1)加入H2O2氧化时,发生反应的化学方程式为________________。
(2)滤渣2的成分是______________(填化学式)。
(3)煅烧过程存在以下反应:2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑ MgSO4+3C=MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体可以是______________(填化学式)。
②B中盛放的溶液可以是______________(填字母)。
A.NaOH溶液 B.Ca(OH)2溶液 C.稀硝酸 D.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com