
| A. | 非金属性:F>Cl>Br>I | B. | 单质氧化性:F2>Cl2>Br2>I2 | ||
| C. | 氢化物稳定性:HF>HCl>HBr>HI | D. | 沸点:F2>Cl2>Br2>I2 |
分析 A、卤族元素中,元素非金属性随着原子序数增大而减弱;
B、卤族元素中,元素非金属性越强,单质氧化性越强;
C、非金属的非金属性越强,其氢化物越稳定;
D.卤族元素中,相对分子质量越大,沸点越高.
解答 解:、卤族元素中,元素非金属性随着原子序数增大而减弱,即非金属性:F>Cl>Br>I,故A不选;
B、卤族元素中,元素非金属性越强,单质氧化性越强,非金属性:F>Cl>Br>I,单质氧化性:F2>Cl2>Br2>I2,故B不选;
C、非金属的非金属性越强,其氢化物越稳定,非金属性:F>Cl>Br>I,氢化物稳定性:HF>HCl>HBr>HI,故C不选;
D.卤族元素中,相对分子质量越大,沸点越高,即沸点:F2<Cl2<Br2<I2,故D选.
故选D.
点评 以卤族元素为例熟练掌握同一主族元素性质递变规律,能从物质结构、原子结构知道其产生递变规律的原因,题目难度不大.


科目:高中化学 来源: 题型:填空题
 ,结构式是F-O-O-O-F.
,结构式是F-O-O-O-F.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②⑤⑥ | C. | ③ | D. | ②④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜作电极电解Na2SO4溶液:Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑ | |
| B. | NH4Al(SO4)2溶液与过量稀氨水反应:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| C. | 用稀硝酸清洗试管内壁的银镜:Ag+2H++NO3-=Ag++NO2↑+H2O | |
| D. | 过量氯气通入碘化亚铁溶液中:2Cl2+2Fe3++2I=4Cl-+2Fe3++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
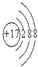

 ,化合物中含有离子键键(填离子或共价)
,化合物中含有离子键键(填离子或共价)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
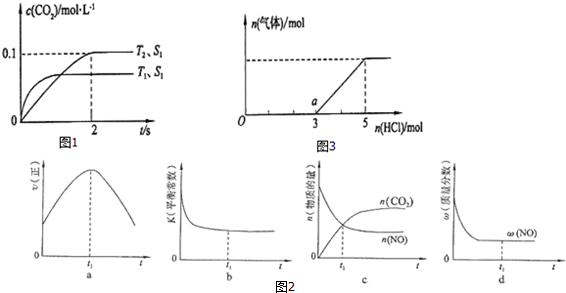
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com