
·ÖĪö £Ø1£©n£ØCl2£©=$\frac{1.12L}{22.4L/mol}$=0.05mol£¬ÓÉ·½³ĢŹ½æÉÖŖĻūŗĵÄHCl£¬·“Ó¦ÖŠHCl²æ·Ö±ķĻÖĪŖĖįŠŌ£¬²æ·Ö±ķĻÖĪŖ»¹ŌŠŌ£¬½įŗĻ·½³ĢŹ½¼ĘĖć£»
£Ø2£©øł¾Żn=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$¼ĘĖćĀČĘųµÄĢå»żŅŌ¼°ĪļÖŹµÄĮ棬½įŗĻ·“Ó¦2Fe+3Cl2=2FeCl3¼ĘĖćŠčŅŖĢśµÄĪļÖŹµÄĮ棬øł¾Żc=$\frac{n}{V}$¼ĘĖćÅØ¶Č£¬ČÜŅŗĻ”ŹĶĒ°ŗó£¬ČÜÖŹµÄĪļÖŹµÄĮæ²»±ä£¬ŅŌ“ĖæɼĘĖćČ”³ö50mL¼ÓĖ®ÅäÖĘ³É200mLČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č£®
½ā“š ½ā£ŗ£Ø1£©n£ØCl2£©=$\frac{1.12L}{22.4L/mol}$=0.05mol£¬ÓÉ·½³ĢŹ½æÉÖŖĻūŗĵÄHClµÄĪļÖŹµÄĮæĪŖ0.2mol£¬·“Ӧɜ³É0.05molĀČĘų£¬ŌņŃõ»Æ0.1molHCl£¬
¹Ź“š°øĪŖ£ŗ0.2 mol£»0.1 mol£»
£Ø2£©n£ØCl2£©=$\frac{42.6g}{71g/mol}$=0.6mol£¬ŌņV£ØCl2£©=0.6mol”Į22.4L/mol=13.44L£¬·¢Éś2Fe+3Cl2=2FeCl3£¬ŌņŠčŅŖĢśµÄĪļÖŹµÄĮæĪŖ0.4mol£¬Éś³É0.4molFeCl3£¬
½«Éś³ÉµÄ¹ĢĢåČ«²æČÜÓŚĖ®£¬Åä³É500mLČÜŅŗ£¬ŌņøĆČÜŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæÅØ¶ČŹĒc£ØFeCl3£©=$\frac{0.4mol}{0.5L}$=0.8mol/L£¬
½«“ĖČÜŅŗČ”³ö50mL¼ÓĖ®ÅäÖĘ³É200mLČÜŅŗ£¬ŌņĘäĪļÖŹµÄĮæÅØ¶ČŹĒ$\frac{0.8mol/L”Į0.05L}{0.2L}$=0.2 mol/L£¬
¹Ź“š°øĪŖ£ŗ13.44L£»0.4 mol£» 0.8 mol/L£» 0.2 mol/L£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹Ō·“Ó¦£¬²ąÖŲÓŚŃõ»Æ»¹Ō·“Ó¦ŅŌ¼°ĪļÖŹµÄĮæÅØ¶ČµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ŅāĻą¹Ų¼ĘĖć¹«Ź½µÄŌĖÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 18gÖŲĖ®ŗ¬ÓŠ10NA øöµē×Ó | |
| B£® | ŹŅĪĀĻĀ£¬42.0gŅŅĻ©ŗĶ±ūĻ©µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżŌ¼ĪŖ3 NA | |
| C£® | ³£ĪĀĻĀ0.05 mol•L-1Fe2£ØS04 £© 3ČÜŅŗÖŠŗ¬Fe 3+ŹżÄæŠ”ÓŚ0.1NA | |
| D£® | ÓƶčŠŌµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®£¬µ±Ņõ¼«µĆµ½2NAøöµē×ÓŹ±Ńō¼«²śÉś22.4 LĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
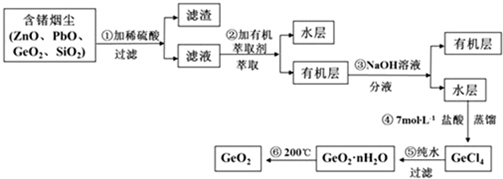
 £Ø3£©µŚ¢Ü²½¼ÓČėŃĪĖį×÷ÓĆÖŠŗĶNaOH£¬×÷·“Ó¦Īļ£¬ŅÖÖĘGeCl4Ė®½ā£Ø“šĮ½µć¼“æÉ£©£®
£Ø3£©µŚ¢Ü²½¼ÓČėŃĪĖį×÷ÓĆÖŠŗĶNaOH£¬×÷·“Ó¦Īļ£¬ŅÖÖĘGeCl4Ė®½ā£Ø“šĮ½µć¼“æÉ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»Æ±µČÜŅŗŗĶĻ”ĮņĖį·“Ó¦£ŗBa2++SO42-=BaSO4”ż | |
| B£® | ÅØŃĪĖįÓėĢśŠ¼·“Ó¦£ŗ2Fe+6H+=2Fe3++3H2”ü | |
| C£® | ĀČĘųĶØČėĖ®ÖŠ£ŗCl2+H2O=2H++Cl-+ClO- | |
| D£® | ÄĘ·ÅÓŚĖ®ÖŠ£ŗ2Na+2H2O=2Na++2OH-+H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
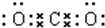 £»¢ŚNaOH
£»¢ŚNaOH £®
£®| Ö÷×å ÖÜĘŚ | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| ¶ž | ¢Ł | ¢Ś | ||||||
| Čż | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | ||
| ĖÄ | ¢į | ¢ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2·Ö×ӱȥżÄ£ŠĶ£ŗ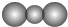 | |
| B£® | ÖŠ×ÓŹżĪŖ21µÄ¼ŲŌ×Ó£ŗ4019K | |
| C£® | NH4IµÄµē×ÓŹ½£ŗ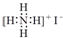 | |
| D£® | HCO3-µÄµēĄė·½³ĢŹ½£ŗHCO3-+H2O?H3O++CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 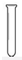 | B£® | 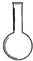 | C£® | 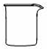 | D£® | 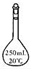 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com