
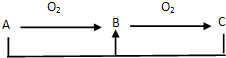
| A、2种 | B、3种 | C、4种 | D、5种 |
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案科目:高中化学 来源: 题型:

| A、根据上述连续实验不能确定溶液X中是否含有Fe3+ |
| B、沉淀H为Al(OH)3、BaCO3的混合物 |
| C、溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- |
| D、若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | Na+ | K+ | Ca 2+ | Mg 2+ | Cl- | SO4 2- | HCO3- |
| 含量/mg?L-1 | 9360 | 83 | 160 | 1100 | 16000 | 1200 | 118 |

查看答案和解析>>
科目:高中化学 来源: 题型:
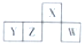 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,且4种元素最外层电子数之和与Ca2+的核外电子数相等.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,且4种元素最外层电子数之和与Ca2+的核外电子数相等.下列判断正确的是( )| A、元素X、Z的原子半径大小:X>Z |
| B、含Y元素的盐溶液有的显酸性,有的显碱性 |
| C、Y、W的简单氢化物中氢元素的化合价相同 |
| D、钙与W可以形成CaW2化合物,且化合物中含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、H2R是二元弱酸,其Ka1=1×10-2 |
| B、当溶液恰好呈中性时,c( Na +)=2c ( R2-)+c( HR-) |
| C、NaHR在溶液中水解倾向大于电离倾向 |
| D、含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| R | ||
| X | M | Y |
| T |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0 mol?L-1 KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、能溶解Al2O3的溶液:Na+、K+、Cl-、SiO32- |
| C、无色透明溶液中:Al3+、Cu2+、Cl-、HCO3- |
| D、使甲基橙变红色的溶液:Mg2+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )| A、VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ |
| B、外电路中电子由c电极流向VB2电极 |
| C、电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D、若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.05mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com