
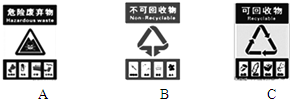

分析 (1)①一次性塑料餐盒属于可回收废品;
②氟氯代烷的大量使用会导致大气平流层的臭氧,1个臭氧分子由3个氧原子构成;
③焦炭与水蒸气反应生成一氧化碳和氢气;
④聚乙烯等材料塑料难以降解,形成白色污染,用可降解材料代替塑料壳减少白色污染;
(2)①塑料为合成的高分子化合物又可称为高分子或巨分子.也是一般所俗称的塑料或树脂;
②钢化玻璃成分其实与普通玻璃相同,光导纤维主要成分是二氧化硅;
③钢化玻璃成分其实与普通玻璃相同,水泥的原料是粘土和石灰石,玻璃的原料是纯碱、石灰石和石英,所以原料中均有石灰石;
(3)①维生素C具有较强的还原性,容易被其他氧化性强的物质氧化;
②小白粉中富含淀粉,油脂在人体中水解最终产物是高级脂肪酸和甘油,胃酸的主要成分是盐酸,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水.
解答 解:(1)①一次性塑料餐盒属于有机塑料类,所以应投入贴有可回收物的垃圾桶内;故答案为:C;
②臭氧能吸收阳光中的紫外线,使人和动物免遭紫外线灼伤,分子式为:O3,故答案为:O3;
③焦炭与水蒸气反应生成一氧化碳和氢气,其反应的方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;故答案为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
④“白色污染”是指塑料污染,所以利用可降解的“玉米塑料”替代聚乙烯塑料制作一次性饭盒,可防止产生“白色污染”,故答案为:白色;
(2)①有机玻璃的成分是有机高分子化合物(聚甲基丙烯酸甲酯),是化学合成的一种塑料,外观颇似玻璃,故选B;
②钢化玻璃成分其实与普通玻璃相同,是一种预应力玻璃,为提高玻璃的强度,通常使用化学或物理的方法,在玻璃表面形成压应力,玻璃承受外力时首先抵消表层应力,从而提高了承载能力,改善了玻璃抗拉强度,石英玻璃的主要成分是二氧化硅,与光导纤维主要成分相同,故选C;
③钢化玻璃成分其实与普通玻璃相同,生产玻璃的原料是纯碱、石灰石和石英,高温下,碳酸钠、碳酸钙和二氧化硅反应分别生成硅酸钠、硅酸钙;
生产水泥以黏土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;所以在玻璃工业、水泥工业中都用到的原料是石灰石,故答案为:石灰石;
(3)①维生素C具有较强的还原性,医用维生素C片在药片外包裹的一层“糖衣”可以防止维生素C被氧化,故答案为:防止维生素C被氧化;
②小白粉中富含淀粉,淀粉属于糖类,植物油属于油脂,油脂在人体中水解最终产物是高级脂肪酸和甘油,胃酸的主要成分是盐酸,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,故答案为:小麦粉;甘油;CaCO3+2H+=Ca2++CO2↑+H2O.
点评 本题考查内容较多,是一道综合题,侧重考查了垃圾分类回收、环境污染、食物中含有六大类营养物质等知识,注意知识的积累和教材知识的灵活应用是解题的关键,题目难度中等.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当今化学研究的方向是研究化学反应中原子的守恒关系 | |
| B. | 光导纤维由硅晶体制成,具有耐腐蚀、传输能力强等特点 | |
| C. | 煤在燃烧过程中要放出大量SO2,是引起光化学烟雾的“罪魁祸首” | |
| D. | 禽流感并不可怕,当加热到70℃以上或使用日常消毒剂都可使其病毒蛋白变性而致死 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4溶液 | B. | HCl溶液 | C. | NaOH溶液 | D. | NaNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| D. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$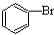 +HBr +HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 断开化学键的过程会放出能量 | |
| B. | 氧化反应均为吸热反应 | |
| C. | 加热才能发生的反应一定是吸热反应 | |
| D. | 放热反应中,反应物的总能量大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠的电子式: | |
| B. | 聚氯乙烯的结构简式: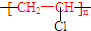 | |
| C. | 硫离子的结构示意图: | |
| D. | 碳酸氢铵的电离方程式:NH4HCO3=NH4++H++CO32ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,O.1 mol•L-1HF溶液pH=l,Ksp(CaF2)随温度和浓度的变化而变化 | |
| B. | 向1L0.2 mol•L-1HF溶液中加入1L O.2 mol•L-1CaCl2溶液,没有沉淀产生 | |
| C. | AgCl不溶于水,不能转化为AgI | |
| D. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于$\frac{1}{\sqrt{1.8}}$×10-11mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com