
【题目】已知1mol氢气和氧气完全燃烧生成水蒸气放出241.8千焦热量,下列热化学方程式正确的是
A. 2H2(g)+O2(g)→2H2O(g)+241.8kJ
B. H2(g)+1/2O2(g)→H2O(s)+241.8 kJ
C. H2(g)+1/2O2(g)→H2O(g)-241.8 kJ
D. H2O(g)→H2(g)+1/2O2(g)-241.8 kJ
【答案】D
【解析】1mol氢气和氧气完全燃烧生成水蒸气放出241.8kJ热量,该反应的热化学方程式为:H2(g)+![]() O2(g)=H2O(g)△H=-241.8kJ/mol,即H2(g)+1/2O2(g)→H2O(g)+241.8 kJ,选项B、C均错误;2mol氢气和氧气完全燃烧生成水蒸气放出483.6kJ热量,该反应的热化学方程式为:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,即2H2(g)+O2(g)→2H2O(g)+483.6kJ,选项A错误;1mol水蒸气分解生成氢气和氧气吸收241.8kJ热量,该反应的热化学方程式为: H2O(g)= H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,即H2(g)+1/2O2(g)→H2O(g)+241.8 kJ,选项B、C均错误;2mol氢气和氧气完全燃烧生成水蒸气放出483.6kJ热量,该反应的热化学方程式为:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,即2H2(g)+O2(g)→2H2O(g)+483.6kJ,选项A错误;1mol水蒸气分解生成氢气和氧气吸收241.8kJ热量,该反应的热化学方程式为: H2O(g)= H2(g)+![]() O2(g)△H=+241.8kJ/mol,即H2O(g)→H2(g)+1/2O2(g)-241.8 kJ,选项D正确。答案选D。
O2(g)△H=+241.8kJ/mol,即H2O(g)→H2(g)+1/2O2(g)-241.8 kJ,选项D正确。答案选D。


科目:高中化学 来源: 题型:
【题目】用X表示原子:
(1)中性原子的中子数:N=________。
(2)阴离子的中子数:AXn-共有x个电子,则N=________。
(3)中性分子中子数:12C18O2分子中,N=________。
(4)A2-原子核内有x个中子,其质量数为m,则n gA2-所含电子的物质的量为________mol。
(5)某元素的同位素X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:X元素在周期表中的位置_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法制取有广泛用途的Na2FeO4,同时获取氢气:Fe+2H2O+2OH-![]() FeO42-+3H2↑,工作原理如图(a)所示,电解质溶液为氢氧化钠溶液,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色色物质。C(Na2FeO4)随初始C(NaOH)的变化如图(b)所示。已知Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法不正确的是
FeO42-+3H2↑,工作原理如图(a)所示,电解质溶液为氢氧化钠溶液,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色色物质。C(Na2FeO4)随初始C(NaOH)的变化如图(b)所示。已知Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法不正确的是
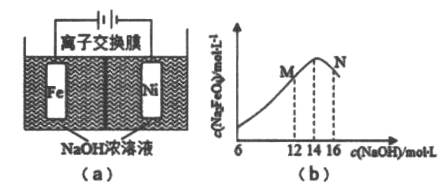
A. 电解一段时间后,阳极室c(OH-)降低
B. 电路中经过0.2mol电子时,阴极室生成H2 2.24L(标准状况)
C. M点C(Na2FeO4)低于最高值的原因是铁电极上有Fe(OH)3生成
D. 阳极的电极反应:Fe一6e-+8OH-===FeO42-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁在某酸雨区的潮湿空气中发生电化学腐蚀,其负极上的反应是
A.O2+2H2O+4e-=4OH-B.2H++2e-=H2↑
C.Fe-2e-=Fe2+D.4OH--4e-=2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】铁、钻、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)基态钴原子的价电子排布式为________,铁、钴、镍的基态原子核外未成对电子数最少的是_____________
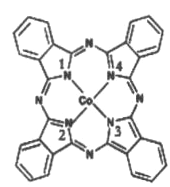
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是__________ (填1、2、3、4),三种非金属原子的电负性由大到小的顺序为____(用相应的元素符号表示);碳原子的杂化轨道类型为_________
(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于_______ (填晶体类型),若配合物Fe(CO) x的中心原子价电子数与配体提供电子数之和为18,则x=_________
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO ______ FeO(填“>”“<”或“=”),原因是___________________________。
(5)NiAs的晶胞结构如图所示:
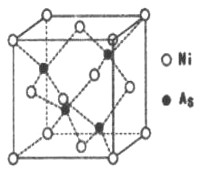
①镍离子的配位数为_________。
②若阿伏加德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为_____cm。(写出计算表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和反应速率的测定。将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
(1)可以判断该分解反应已经达到平衡的是________。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
E.单位时间内消耗1 molNH2COONH4 ,同时生成2mol NH3
F.密闭容器中混合气体的平均摩尔质量不变 G.容器内NH3与CO2的浓度之比为2∶1 H.6个N—H键断裂的同时,有2个C=O键形成
(2)根据表中数据,计算25.0 ℃时的分解平衡常数______________。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量________(填“增加”、“减少”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定一种气态烃A的化学式,取一定量的A置于一密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的最简式,他们测得的在一定条件下的有关数据如下(图中的箭头表示气流的方向,实验前系统内的空气已排尽):
甲方案:燃烧产物![]() 浓硫酸增重2.52 g
浓硫酸增重2.52 g![]() 碱石灰增重1.32g
碱石灰增重1.32g![]() 生成CO21.76 g
生成CO21.76 g
乙方案:燃烧产物![]() 碱石灰增重5.60 g
碱石灰增重5.60 g![]() 固体减小0.64 g
固体减小0.64 g![]() 石灰水增重4g。试回答:
石灰水增重4g。试回答:
(1)甲、乙两方案中,你认为哪种方案能求出A的最简式_______?
(2)请根据你选择的方案,通过计算求出A的最简式_______。(要求写出计算过程)
(3)若要确定A的分子式,是否需要测定其它数据?并说明原因_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com