
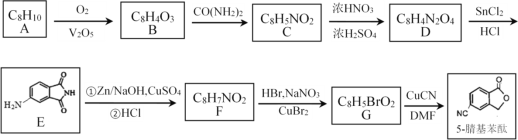
����Ŀ��ij�о�С����ϳɿ�����ҩ��̪�����м��� 5-�����̪��
��֪����![]()
![]()
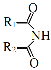 ��
��![]()
![]()
![]()
��ش�
(1)����˵����ȷ����______��
A�������� C ����������
B�������� D ������������
C���� B��C��F��G�����Ķ���ȡ����Ӧ
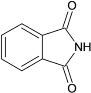
D��5-�����̪�ķ���ʽΪ C9H4NO2
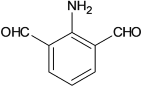
(2)������ F �Ľṹ��ʽ��______��
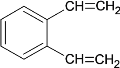
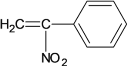
(3)д�� A��B �Ļ�ѧ����ʽ______��
(4)�������Ȳ������Ϊԭ�ϣ����Լ���ѡ���Ʊ� C �ĺϳ�·��______��
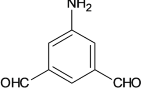
(5)д�������� F��C8H7NO2��ͬʱ��������������ͬ���칹��Ľṹ��ʽ______��
1H��NMR��IR��������
�ٷ������� 4 �ֻ�ѧ������ͬ����ԭ��
�ڷ����к�������û���ǻ�������������O��O����
�۳���������������״�ṹ
���𰸡�AC 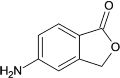
 +3O2
+3O2![]()
 +3H2O CH��CH
+3H2O CH��CH![]()
![]()
![]()
![]()

![]()
 ��
�� ��
��![]() ��
�� ��
��
��������
��A�ķ���ʽ�����E�Ľṹ��ʽ���ݹ���������û�����뱽�����Լ����룬��A���б�������AΪ ���Ա�A��B�ķ���ʽ����֪A����������Ӧ����B�������Ϣ�ٿ�֪��A�м�ת��Ϊ��COOH��2���Ȼ�֮����ȥ1����ˮ�õ�B����BΪ
���Ա�A��B�ķ���ʽ����֪A����������Ӧ����B�������Ϣ�ٿ�֪��A�м�ת��Ϊ��COOH��2���Ȼ�֮����ȥ1����ˮ�õ�B����BΪ ����CΪ
����CΪ ��C����ȡ����Ӧ����DΪ
��C����ȡ����Ӧ����DΪ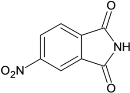 �������Ϣ�ڿ�֪��D������ԭ��Ӧ����E����F��G�ķ���ʽ��֪��E����ϼ���1��NH��F��F���1����NH2����Br����õ�G�����5-�����̪�ṹ��֪��G�У�Br����CN���ת��Ϊ5-�����̪����FΪ
�������Ϣ�ڿ�֪��D������ԭ��Ӧ����E����F��G�ķ���ʽ��֪��E����ϼ���1��NH��F��F���1����NH2����Br����õ�G�����5-�����̪�ṹ��֪��G�У�Br����CN���ת��Ϊ5-�����̪����FΪ ��GΪ
��GΪ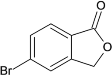 ��
��
(1)A��CΪ �������백�����ƵĽṹ�����������ԣ�A��ȷ��
�������백�����ƵĽṹ�����������ԣ�A��ȷ��
B��DΪ ������1��������B����
������1��������B����
C�������ʽṹ��֪����B��C��F��G�����Ķ���ȡ����Ӧ��C��ȷ��
D��5�������̪�ķ���ʽΪC9H5NO2��D����
��ΪAC��
(2)�ɷ�����֪��������F�Ľṹ��ʽ�ǣ� ��
��
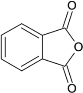
(3)A��B�Ļ�ѧ����ʽΪ�� +3O2
+3O2![]()
 +3H2O��
+3H2O��
(4)��Ȳ��ϳɱ���������Ȳ�����ӳɷ�Ӧ�õ� ��Ȼ�������Ը��������Һ��������ˮ�õ�
��Ȼ�������Ը��������Һ��������ˮ�õ� ����������ط�Ӧ�õ�
����������ط�Ӧ�õ� ���ϳ�·������ͼΪ��CH��CH
���ϳ�·������ͼΪ��CH��CH![]()
![]()
![]()

![]()

![]()
 ��
��
(5)������F(C8H7NO2)ͬʱ��������������ͬ���칹�壺�ٷ�������4�ֻ�ѧ������ͬ����ԭ�ӣ��ڷ����к�������û���ǻ���������(��O��O��)���۳���������������״�ṹ������F�ķ���ʽ�ͽṹ��ʽ����ͬ���칹�����ͬC��Nԭ�ӵı����л�������12��Hԭ�ӣ����б�������8����˵�������ϻ���Ҫ��4��Hԭ�ӣ��������2����CHO��Ҳ����1����NO2��1��̼̼˫������������4�ֻ�ѧ������ͬ��Hԭ�ӣ�˵���Գ��Խϸߣ������������ͬ���칹��Ϊ�� ��
�� ��
��![]() ��
�� �ȡ�
�ȡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫���绯ѧ��(װ����ͼ)���ڴ�ͳ���װ���з����˵����Ե缫BPE��ͨ��ʱ��BPE���˽���������Ʋ�����ݶȺϽ������й�˵���������

A.mΪ��Դ����
B.BPE��b�˱�a�˵ĵ��Ƹ�
C.BPE��a�˷����ķ�ӦΪ�� 2H2O+2e-=H2��+2OH-
D.BPE��b�˵����ĵIJ�ͬλ�ã����γ���ɲ�ͬ��ͭ���Ͻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ҹ��Ĵ�ͳ��Ʒ����Ҷ�к��еIJ��ӿ������ʳƷ���Ӽ��ж������к��ĺϳɿ������������ڶ���ʳƷ���ʵȣ���ͼ��ʾ�Dz����к�����ߵ�һ�ֶ�����A�Ľṹ��ʽ���������ֶ�����A���й�������ȷ����( )
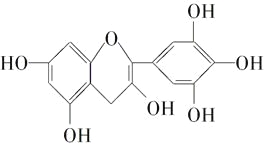
�ٷ���ʽΪC15H12O7
��1 mol������A��һ���������������7 molH2�ӳ�
�۵������Ķ�����A�ֱ��������Ľ����ƺ��������Ʒ�Ӧ�����Ľ����ƺ��������Ƶ����ʵ���֮��Ϊ1��1
��1 mol������A��������Ũ��ˮ��Ӧ���������4 mol Br2
A.�٢�B.�٢�C.�ڢ�D.�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������(����)
A.![]() H��
H��![]() H��H����H2����Ԫ�ص����ֲ�ͬ����
H��H����H2����Ԫ�ص����ֲ�ͬ����
B.![]() Ca��
Ca��![]() Ca�����ֲ�ͬ��Ԫ��
Ca�����ֲ�ͬ��Ԫ��
C.![]() H��
H��![]() H�Dz�ͬ�ĺ���
H�Dz�ͬ�ĺ���
D.![]() C��
C��![]() C��
C��![]() C��Ϊͬλ�أ��������ʲ�ͬ������ѧ���ʼ�����ȫ��ͬ
C��Ϊͬλ�أ��������ʲ�ͬ������ѧ���ʼ�����ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���ô���(��Ca2����Mg2����![]() ������)Ϊ��Ҫԭ�ϲ����������Ƽ����������ͻ���NH4Cl��������������ͼ��ʾ�������й�˵����ȷ����(����)
������)Ϊ��Ҫԭ�ϲ����������Ƽ����������ͻ���NH4Cl��������������ͼ��ʾ�������й�˵����ȷ����(����)
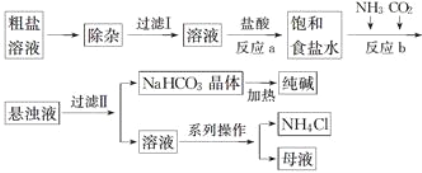
A. ���������Ƽ�����漰����������ԭ��Ӧ
B. ����ʳ��ˮ����ͨ�������ΪCO2
C. ����ͼ�е�ϵ�в�����һ����Ҫ������
D. ������ֻ��̼�����Ƽ��ȷֽ������CO2�ɻ���ѭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�������̶����ܱ������з������淴Ӧ3X(g)![]() 2Y(g)+Z(g)��������˵���ﵽ��ѧƽ��״̬����
2Y(g)+Z(g)��������˵���ﵽ��ѧƽ��״̬����
A.ѹǿ���ٷ����仯B.��H����ֵ���ٱ仯
C.��Ӧ����������Ũ�Ȳ��ٸı�D.Y������������Z���������ʵ�2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H7N9����������ȫ���״η��ֵ����������в�������ƣ�Tamiflu�������Ƹò��������ҩ���ç����Ϊԭ�ϣ����ಽ��Ӧ���Ƶô�ƺͶ��ǻ������ᣮ��ơ�ç���ᡢ���ǻ�������Ľṹ��ʽ���£�

�����й�˵����ȷ���ǣ� ��
A. ��ơ�ç���ᡢ���ǻ������ᶼ���ڷ����廯����
B. 1molç������NaOH��Һ��Ӧ���������4mol NaOH
C. ���ǻ���������ȶ����ڿ����в��ױ�����
D. ����FeCl3��Һ������ç����Ͷ��ǻ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾת����ϵ��A��B��C��Ϊ˫ԭ����̬���ʣ��ֱ��ɶ���������Ԫ��X��Y��Z��ɡ����е���B�����õ��Ӷ�����࣬�ͱ������о�����10�����ӡ�����˵���������
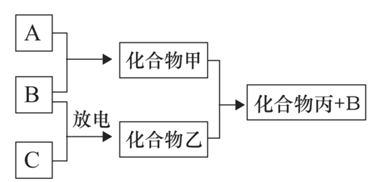
A.ZԪ��λ�ڵڶ����ڵ�VIA��
B.������ˮ���ռ���������
C.�����£�pH=12�Ļ������ˮ��Һ�У�ˮ�������c(H+)=10��12mol��L��1
D.����������ڻ�������У����ڵ�����4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2C2O4Ϊ��Ԫ���ᣬ�Ҿ��л�ԭ�ԡ�
����20��ʱ���ı�0.1mol��L��1H2C2O4��Һ��pH����Һ�е�H2C2O4��HC2O4����C2O42�������ʵ���������(X)��pH�ı仯��ͼ��ʾ��
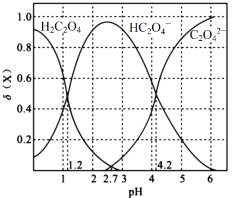
��֪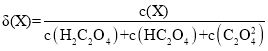
��1��Ka1(H2C2O4)��___________��
��2��0.1mol��L��1NaHC2O4��Һ������Ũ���ɴ�С��˳����___________��
��3����֪20��ʱK(HCOOH)=1.77��10-4����HCOONa��Һ�м�������H2C2O4����Ӧ�����ӷ���ʽ��___________��
����KMnO4��Һ������������ԭ��Ӧ�ζ��ı�Һ������KMnO4��ǿ�����ԣ�������Һ�����ױ������л�ˮ�е�ijЩ������ԭ�����ʻ�ԭ�����ʹ��ǰ����H2C2O4��2H2O���Ƶı���Һ�궨����֪��5H2C2O4+2KMnO4+3H2SO4=10CO2��+2MnSO4+K2SO4+8H2O����
��4��ȷ��ȡһ�������KMnO4��Һ��Ҫʹ�õ�������____________��
��5��ijѧ������3��ʵ��ֱ��¼�й����������ʾ����KMnO4��Һ�����ʵ���Ũ��Ϊ___________mol��L��1��
ʵ����� | ����0.1000mol��L��1��H2C2O4��Һ�����/mL | ����KMnO4��Һ�����/mL |
1 | 29.90 | 25.00 |
2 | 30.00 | 25.00 |
3 | 30.10 | 25.00 |
��6���������ζ������У����������ɵ��±��ⶨ��KMnO4Ũ��ƫ�ߵ���___________
a��δ�ñ�Һ��ϴ�ζ���
b���ﵽ�ζ��յ㣬����ʱ����Һ��
c��ʢװ����Һ����ƿ������ˮϴ����δ��ϴ
d���ζ�ǰ�ζ����¶˼����������ݣ��ζ���������ʧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com