
【题目】我国国家标准(GB2760)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
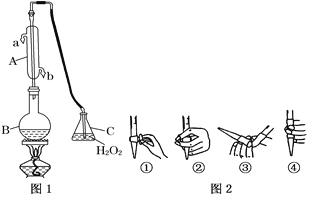
(1)仪器A的名称是__________,水通入A的进口为________。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为_____________________________。
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的______;若滴定终点时溶液的pH=8.8,则选择的指示剂为______;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)__________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:________g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施: ____________。
(6)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,若吸收后的吸收液恰好呈中性,下列关于该吸收液的说法正确的是______________________。
A.c(Na+)=c(HSO3-)+2c(SO32-) |
B.c(Na+)>c(HSO3-)=c(SO32-)>c(H+) = c(OH-) |
C.2c(Na+)=3c(H2SO3)+3c(HSO3-)+3c(SO32-) |
D.c(Na+)>c(HSO3- ) + c(SO32-) +c(H2SO3) |
【答案】直形冷凝管 b SO2+H2O2=H2SO4 ③ 酚酞 ④ 0.24 原因:盐酸的挥发; 改进措施:用不挥发的强酸如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响 AD
【解析】
测定葡萄酒中二氧化硫的含量,首先把葡萄酒和适量盐酸放入B中,加热使二氧化硫全部逸出进入H2O2中被吸收,生成硫酸(H2O2+SO2=H2SO4),然后用中和滴定的方法测定硫酸的浓度,进而计算二氧化硫的含量。盐酸的作用是促使二氧化硫逸出,但盐酸本身也有挥发性,对中和滴定结果有影响,所以应把盐酸换成硫酸。
(1)根据仪器A的构造可知,仪器A为直形冷凝管,冷凝管中通水方向采用逆向通水法,冷凝效果最佳,所以应该进水口为b;
(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的化学方程式为:SO2+H2O2=H2SO4;
(3)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用③的方法;滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0);若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,滴定管的0刻度在上方,10mL刻度线下方还有40mL有刻度的溶液,另外滴定管50mL刻度线下有液体,因此管内的液体体积>(50.00mL-10.00mL)=40.00mL,所以④正确;
(4)根据2NaOH~H2SO4~SO2可知SO2的质量为:![]() ×(0.0900mol/L×0.025L)×64g/mol=0.072g,该葡萄酒中的二氧化硫含量为:
×(0.0900mol/L×0.025L)×64g/mol=0.072g,该葡萄酒中的二氧化硫含量为:![]() =0.24g/L;
=0.24g/L;
(5)由于盐酸是挥发性酸,挥发的酸消耗氢氧化钠,使得消耗的氢氧化钠溶液体积增大,测定结果偏高;因此改进的措施为:用不挥发的强酸,如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响;
(6)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,吸收后的吸收液恰好呈中性,c(H+)=c(OH-),依据溶液中电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32-),得到c(Na+)=c(HSO3-)+2c(SO32-),A正确;若c(HSO3-)=c(SO32-),溶液呈碱性c(H+)<c(OH-),故B错误;由物料守恒可知亚硫酸氢钠和亚硫酸钠按照1:1混合,溶液呈碱性,溶液中物料守恒为:2c(Na+)=3c(H2SO3)+3c(HSO3-)+3c(SO32-),但由于溶液呈中性,亚硫酸氢钠和亚硫酸钠的物质的量不同,故C错误;依据化学式可知,亚硫酸氢钠中硫元素物质的量和钠元素的物质的量相同,亚硫酸钠中钠元素的物质的量大于亚硫酸根中硫元素的物质的量,所以c(Na+)>c(HSO3-)+c(SO32-)+c(H2SO3),故D正确。


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。查阅资料知SO3的熔点为16.83℃,沸点是44.8℃。某化学学习小组欲通过实验测定上述反应中SO2的转化率,他们设计了如下实验。
2SO3(g) ΔH<0。查阅资料知SO3的熔点为16.83℃,沸点是44.8℃。某化学学习小组欲通过实验测定上述反应中SO2的转化率,他们设计了如下实验。

请根据要求回答问题:
(1)各装置接口的连接顺序是a→__。
(2)装置Ⅳ烧杯中盛放冰水的作用是__。
(3)装置Ⅰ所用硫酸,一般选用浓度为70%~80%的硫酸,原因是__。
(4)当装置Ⅰ中反应结束时,要打开止水夹继续通入O2一段时间,继续通入O2的目的是__。
(5)称量agNa2SO3粉末与足量硫酸反应,实验结束后称得装置Ⅳ增重bg,列式表示该实验中SO2的转化率__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关W、X、Y、Z、R五种元素的叙述正确的是( )
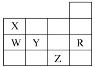
A. 常温下,Z的单质为气态物质
B. Y、Z的阴离子的电子层结构都与R原子的相同
C. W的氢化物的稳定性要比X的强
D. Y的元素的非金属性比W元素强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数大于4的主族元素Xm+、Yn-的离子核外电子层结构相同,则关于X、Y两元素的叙述正确的是
A. X的原子序数小于Y的原子序数 B. X、Y的核电荷数之差是(m-n)
C. X和Y处于同一周期 D. Y元素与X元素的族序数之差是8-(m+n)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H14O4的有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则符合该条件的有机物有( )(不考虑立体异构)
A.8种B.10种C.13种D.16种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 是原子序数依次增大的五种短周期元素,且
是原子序数依次增大的五种短周期元素,且![]() 是元素周期表中原子半径最小元素,
是元素周期表中原子半径最小元素,![]() 、
、![]() 相邻,
相邻,![]() 元素可以与
元素可以与![]() 、
、![]() 、
、![]() 元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子双原子化合物。
元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子双原子化合物。![]() 元素原子的最外层电子数与核外电子层数相等。已知:甲+丙→丁。下列说法正确的是
元素原子的最外层电子数与核外电子层数相等。已知:甲+丙→丁。下列说法正确的是
A.简单离子半径:![]()
B.![]() 与
与![]() 两种元素共同形成的10电子微粒有3种
两种元素共同形成的10电子微粒有3种
C.![]() 元素在元素周期表中的位置是第二周期第ⅡA族
元素在元素周期表中的位置是第二周期第ⅡA族
D.丁物质由非金属元素组成,只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雕白块(NaHSO2·HCHO·2H2O,易溶于水,呈白色块状固体或结晶性粉状)可用作印染工业的还原剂、橡胶合成及制糖工业中的漂白剂。以SO2、纯碱、Zn及甲醛为原料生产雕白块及氧化锌的工艺流程如下:
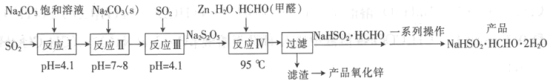
回答下列问题:
(1)NaHSO2·HCHO·2H2O中S元素的化合价为__________。
(2)“反应I”中得到的产物是__________(填化学式)。
(3)设计“反应II”,“反应III”中继续通入SO2的目的是_________。
(4)“反应Ⅳ”的化学方程式为______________。
(5)“过滤”后,“滤渣”是__________(填化学式)。
(6)“一系列操作”包括蒸发浓缩________、________、________干燥。
(7)一种测定雕白块中硫的质量分数的方法如下:称取a g产品溶于适量水中,加入稍过量的碘水(反应生成NaHSO4和HCOOH),充分反应后加入足量BaCl2溶液,过滤,滤渣经干燥后称得质量为b g。
①雕白块与碘水反应的化学方程式为___________。
②产品中硫的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10 L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图甲,C的百分含量与温度的关系如图乙。
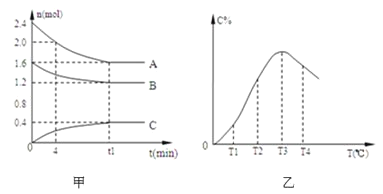
下列分析不正确的是( )
A.0~4 min时,A的平均反应速率为0.02 mol·L-1·min-1
B.该反应的化学方程式为2A(g)+B(g)C(g)
C.由T1向T2变化时,正反应速率大于逆反应速率
D.该反应正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各实验装置的叙述正确的是( )
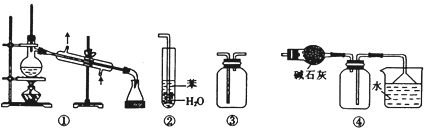
A. 装置①常用于分离互不相溶的液体混合物
B. 装置②用于吸收NH3或HCl气体时,易形成倒吸
C. 装置③可用于收集H2、CO2、Cl2、NH3、C2H4等气体
D. 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com