
| A. | 含有共价键的晶体,一定是原子晶体 | |
| B. | 离子晶体中,一定存在金属元素和非金属元素 | |
| C. | 同时含有离子键和共价键的化合物,既可能是离子化合物,也可能是共价化合物 | |
| D. | 在共价化合物中一定存在共价键,但含有共价键的不一定是共价化合物 |
分析 A.由分子构成的物质可存在共价键;
B.离子晶体中可能不含金属元素;
C.含离子键的一定为离子化合物;
D.共价键可存在于共价化合物或离子化合物中.
解答 解:A.由分子构成的物质可存在共价键,则含有共价键的晶体,可能为分子晶体、原子晶体,故A错误;
B.离子晶体中可能不含金属元素,如铵盐中不含金属元素,故B错误;
C.含离子键的一定为离子化合物,则含离子键的不可能为离子化合物,故C错误;
D.共价键可存在于共价化合物或离子化合物中,则在共价化合物中一定存在共价键,但含有共价键的不一定是共价化合物,故D正确;
故选D.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意化合物中的化学键,题目难度较大.


科目:高中化学 来源: 题型:解答题

| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8(>8溶解) | 9(>9溶解) |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
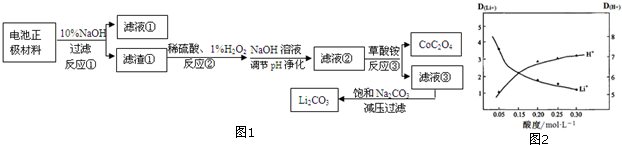
| 弱电解质 | CoC2O4 | Fe(OH)3 | NH3•H2O | H2C2O4 |
| 平衡常数 | Ksp=6.3×10-8 | Ksp=2.79×10-39 | Ka=1.7×10-5 | Ka1=5.6×10-2 Ka2=5.4×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶粒可以透过滤纸,不能透过半透膜 | |
| B. | 采用喷雾型药剂形成一定大小的液珠,可有效提高药物疗效 | |
| C. | 冶金工业的矿粒除尘利用了丁达尔效应 | |
| D. | 空气中的雾压现象体现了胶体的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 CH2-CHCl
CH2-CHCl .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密度:苯<水<溴苯 | B. | 沸点:戊烷>2-甲基丁烷>丙烷 | ||
| C. | 酸性:HCO3-<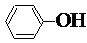 <H2CO3 <H2CO3 | D. | 与Na反应的速率:水>苯酚>乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,CCH3CH3,D
,CCH3CH3,D .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com