
���� ��1����������һ�����ʵ���Ũ����Һһ�㲽��ѡ����Ҫ������ȱ�ٵIJ�����
��2���������������ʵ����ʵ�������Һ�����Ӱ�죬����C=$\frac{n}{V}$������������
��� �⣺��1���ù�������һ�����ʵ���Ũ����Һ��һ�㲽�裺���㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȣ��õ���������������ƽ��ҩ�ס��ձ���100mL����ƿ������������ͷ�ιܣ����Եڶ����ܽ��������Ҫ�õ����������ձ������������ܽ����ϴ�ӡ����ݡ�ҡ�Ⱥɵ�������Һ��
�ʴ�Ϊ���ձ�����������100mL����ƿ�����ݣ�
��2��A����������������ϣ�BaCl2���������Ͻ��г�����ʵ�ʳ�������ƫС�����ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ���Aѡ��
B��ѡ�õ�����ƿ������������ˮ�������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ�Ȳ��䣬��B��ѡ��
C������ҡ�Ⱥ�Һ���½����ּ�ˮ���̶��ߣ�������Һ���ƫ����ҺŨ��ƫ�ͣ���Cѡ��
D���ȼ�������ܶȽϴ���Ȼ�����Һ��������ϴ���ձ��Ͳ���������Һ�ܶȽ�С�������Һ�ܶȲ����ȣ����ҡ�����ܶȴ�ĺ��ܶ�С�����������ȶ���ԭ���֮��С����������ҺŨ��ƫ��D��ѡ��
��ѡ��AC��
���� ���⿼��һ�����ʵ���Ũ����Һ�����ƣ��ѶȲ�����ȷ����ԭ���ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��ԭ�ӽṹʾ��ͼ��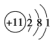 | |
| B�� | ����6�����Ӻ�7�����ӵ�̼Ԫ�صĺ��ط��ţ�${\;}_{6}^{13}$C | |
| C�� | �����ĵ���ʽ����N������N�� | |
| D�� | �õ���ʽ��ʾ�����Ƶ��γɹ��̣�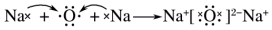 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molFeCl3���ˮ��Ӧ���ɽ������NA��Fe��OH��3���� | |
| B�� | 25�桢1.01��105 Pa�£�44g CO2�к��е�ԭ����Ϊ3NA | |
| C�� | 1 L 0.5mol/L Na2CO3 ��Һ�к��е�CO32-��ĿΪ0.5NA | |
| D�� | 1 mol Cl2������Fe��Ӧ��ת�Ƶĵ�����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
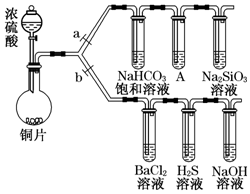 ����Ҫ���������ʵ����̣�a��bΪ���ɼУ����ȼ��̶�װ������ȥ����
����Ҫ���������ʵ����̣�a��bΪ���ɼУ����ȼ��̶�װ������ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��s��+O2��g����SO2��g�� Q1 kJ�� S��g��+O2��g����SO2��g�� Q2 kJ | |
| B�� | 2H2��g��+O2��g����2H2O��g�� Q1kJ�� 2H2��g��+O2��g����2H2O��l�� Q2kJ | |
| C�� | NaOH��aq��+HCl��aq����NaCl��aq��+H2O��l�� Q1kJ�� NaOH��aq��+CH3COOH��aq����CH3COONa��aq��+H2O��l�� Q2 kJ | |
| D�� | H2��g��+Cl2��g����2HCl��g�� Q1kJ�� H2��g��+F2��g����2HF��g�� Q2kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ������������Һ�����ʱ��Һ�岻����������$\frac{2}{3}$ | |
| B�� | �������ʱ���������н�����ˮӦ�ǡ��½��ϳ��� | |
| C�� | ʢ��NaOH��Һʱ��ʹ�ô�������ĥ��ƿ | |
| D�� | ��ȡ����ʱ��Ӧѡ���л���ȡ��������ȡ�����ܶȱ�ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | �� | 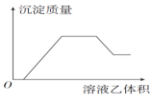 | |
| A | NH4NO3��Al��NO3��3��HCl��Fe��NO3��3 | NaOH | |
| B | Na2CO3��NH4HCO3��Na2SO4 | Ba��OH��2 | |
| C | AlCl3��Mg��NO3��2��HNO3 | NaOH | |
| D | NaAlO2��NH3•H2O��NaOH | H2SO4 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
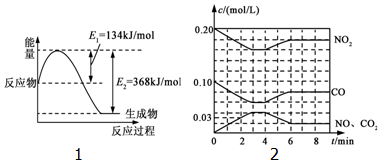 ���Ŵ�����Ⱦ���������أ������ܼ��š�������ȫ�����������ŷţ��о�NOx��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壮
���Ŵ�����Ⱦ���������أ������ܼ��š�������ȫ�����������ŷţ��о�NOx��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com