
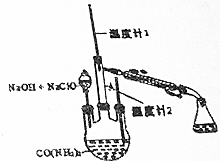
 水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:
水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:分析 (1)配制一定质量分数的溶液所需玻璃仪器为量筒、烧杯、玻璃棒;
(2)C12通入30%Na0H溶液生成NaC1O、NaC1和水;
(3)根据反应N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl进行判断;
(4)实验时可根据N2H4•H2O沸点判断将N2H4•H2O开始蒸出;
解答 解:(1)配制一定质量分数的溶液所需玻璃仪器为量筒、烧杯、玻璃棒,故选BD;
(2)C12通入30%Na0H溶液生成NaC1O、NaC1和水,反应的方程式为C12+2Na0H=NaC1O+NaC1+H2O,
故答案为:C12+2Na0H=NaC1O+NaC1+H2O;
(3)根据反应N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl可知,如果将NaOH和NaClO的混合溶液一次性加入三颈烧瓶,可能会使生成的N2H4•H2O被氧化,造成N2H4•H2O产率下降,
故答案为:使生成的N2H4•H2O被氧化,造成N2H4•H2O产率下降;
(4)实验时可根据N2H4•H2O沸点判断将N2H4•H2O开始蒸出,即根据温度计1中测得的温度判断,
故答案为:温度计1中测得的温度;
点评 本题考查物质制备实验,涉及氧化还原反应、对装置与操作的分析评价、物质分离提纯等,关键是对题目信息的理解应用,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 序号 | 反应 温度/℃ | c(HCl)/ mol•L-1 | v(HCl) /mL | 碳酸钙的形状 | t/min |
| 1 | 20 | 2 | 10 | 块状 | t1 |
| 2 | 20 | 2 | 10 | 粉末 | t2 |
| 3 | 20 | 4 | 10 | 粉末 | t3 |
| 4 | 40 | 2 | 10 | 粉末 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Na+、SO42-、Ba2+ | B. | K+、Na+、HCO3-、NO3- | ||
| C. | OH-、HCO3-、Ca2+、Na+ | D. | Ba2+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
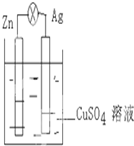 如图,在银锌原电池中,以硫酸铜溶液为电解质溶液.
如图,在银锌原电池中,以硫酸铜溶液为电解质溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足8电子稳定结构 | |
| B. | P4和CH4都是正四面体分子且键角都为109°28ˊ | |
| C. | s轨道与s轨道之间可以在任何方向上成键,所以共价键都没有方向性 | |
| D. | s轨道与p轨道只有沿着一定的方向,才能发生最大程度的重叠,形成共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com